题目内容
下列各组离子一定可以大量共存的是( )
| A、在含大量Al3+的溶液中:NH4+、Na+、HCO3-、SO42- |
| B、能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、Cl- |
| C、在水电离出的c(H+)=10-13mol?L-1 的溶液中:NH4+、AlO2-、SO42-、NO3- |
| D、加Al粉能放H2的溶液中:K+、Na+、Cl-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.含有大量Al3+的溶液中不能大量存在和铝离子反应的离子;
B.能使甲基橙试液变红的溶液为酸性,和氢离子反应的离子不能大量共存;
C.在水电离出的c(H+)=10-13mol?L-1 的溶液呈酸性或碱性,则和氢离子或氢氧根离子反应的离子不能大量共存;
D.加Al粉能放H2的溶液为非氧化性酸或碱溶液.
B.能使甲基橙试液变红的溶液为酸性,和氢离子反应的离子不能大量共存;
C.在水电离出的c(H+)=10-13mol?L-1 的溶液呈酸性或碱性,则和氢离子或氢氧根离子反应的离子不能大量共存;
D.加Al粉能放H2的溶液为非氧化性酸或碱溶液.
解答:
解:A.Al3+和HCO3-发生双水解反应,所以不能大量共存,故A错误;
B.能使甲基橙试液变红的溶液为酸性,MnO4-、Cl-发生氧化还原反应而不能大量共存,故B错误;
C.在水电离出的c(H+)=10-13mol?L-1 的溶液呈酸性或碱性,NH4+和氢氧根离子反应生成弱电解质、AlO2-和氢离子反应生成氢氧化铝,所以不能大量共存,故C错误;
D.加Al粉能放H2的溶液为非氧化性酸或碱溶液,这几种离子和氢离子或氢氧根离子都不反应,所以能大量共存,故D正确;
故选D.
B.能使甲基橙试液变红的溶液为酸性,MnO4-、Cl-发生氧化还原反应而不能大量共存,故B错误;
C.在水电离出的c(H+)=10-13mol?L-1 的溶液呈酸性或碱性,NH4+和氢氧根离子反应生成弱电解质、AlO2-和氢离子反应生成氢氧化铝,所以不能大量共存,故C错误;
D.加Al粉能放H2的溶液为非氧化性酸或碱溶液,这几种离子和氢离子或氢氧根离子都不反应,所以能大量共存,故D正确;
故选D.
点评:本题考查离子共存,为高考高频点,明确离子性质及离子共存条件是解本题关键,还常常与盐类水解、氧化还原反应、离子颜色、溶液pH等联合考查,易错选项是C.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
已知:①金属钠燃烧火焰呈黄色;②灼烧KCl火焰呈紫色;③硫磺在纯氧中燃烧火焰呈蓝紫色;④甲烷燃烧火焰呈淡蓝色.在上述四个反应中属于焰色反应的是( )
| A、只有② |
| B、只有①② |
| C、只有 ②③ |
| D、①②③④ |
元素及其化合物丰富了物质世界,下列说法正确的是( )
| A、常温下把Cu放入冷的浓H2SO4中无明显现象,是因为Cu在冷的浓H2SO4中会钝化 |
| B、NaOH溶液和A1Cl3溶液相互滴加的现象不同 |
| C、金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| D、Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与H2O发生反应 |
在523K时,有以下反应:2HCl(g)+CrO3(g)═CrO2Cl2(g)+H2O(g)+Q (Q>0),反应进行至第5min时,改变某个条件,当反应进行至第10min时,发现生成CrO2Cl2(g)的速率增大,CrO2Cl2的百分含量也增大,则改变的条件不可能是( )
| A、加热 | B、使用催化剂 |
| C、加压 | D、分离出水气 |
甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是( )
| A、甲中水电离出来的H+ 的物质的量浓度是乙中水电离出来的H+ 的物质的量浓度的10倍 |
| B、中和等物质的量的NaOH溶液需甲、乙两杯醋酸溶液的体积,10V(甲)>V(乙) |
| C、物质的量浓度c(甲)>10c(乙) |
| D、甲中的c(OH-)为乙中的c(OH-)的10倍 |
钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为W(s)+2I2(g)
WI4(g).下列说法正确的是( )
| 1400℃ |
| 约3000℃ |
| A、温度越高,灯丝的使用寿命越长 |
| B、WI4在灯丝上分解,产生的W又沉积在灯丝上 |
| C、WI4在灯管壁上分解,使灯管的寿命延长 |
| D、温度升高时,WI4的分解速率加快,W和I2的化合速率减慢 |
下列化合物含有离子键的是( )
| A、H2O |
| B、NH3 |
| C、CaCl2 |
| D、CH4 |
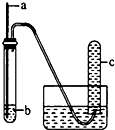 用如图装置实验,下列实验现象预期及相应结论均正确的是( )
用如图装置实验,下列实验现象预期及相应结论均正确的是( )