题目内容
某同学用Na2SO3粉末与浓H2SO4制备并收集SO2,用盛有NaOH溶液的烧杯吸收多余的SO2,实验结束后烧杯中溶液无明显现象,现对其成分进行探究.
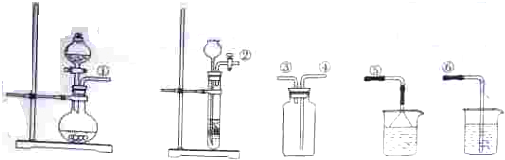
(1)选择合适的仪器并按从左到右的顺序连接:
(2)假设溶液中同时存在Na2SO3和NaOH,设计实验方案,进行成分检验.在答题卡上写出实验步骤、预期现象和结论.仪器任选,限选试剂:
稀盐酸、稀硝酸、铁丝、铜丝、CaCl2溶液、品红溶液、酚酞、甲基橙
(3)若溶液中同时存在Na2SO3和NaHSO3,为了准确测定溶液的浓度,实验如下:
①原理:SO32-+I2+H2O═SO42-+2I-+2H+
HSO3-+I2+H2O═SO42-+2I-+3H+
②步骤:准确量取10.00mL溶液于锥形瓶中,滴加几滴淀粉溶液,用0.1000mol/L碘液滴定至终点,消耗碘液20.00mL;再用0.2000mol/L NaOH溶液滴定生成的酸,消耗NaOH溶液23.00mL.
③计算:c(Na2SO3)= mol/L,c(NaHSO3)= mol/L.

(1)选择合适的仪器并按从左到右的顺序连接:
(2)假设溶液中同时存在Na2SO3和NaOH,设计实验方案,进行成分检验.在答题卡上写出实验步骤、预期现象和结论.仪器任选,限选试剂:
稀盐酸、稀硝酸、铁丝、铜丝、CaCl2溶液、品红溶液、酚酞、甲基橙
| 实验步骤 | 预期现象和结论 |
| 步骤1: | 火焰呈黄色,证明原溶液中存在Na+. |
| 步骤2: | |
| 步骤3:另取少量原溶液于试管中, | 品红溶液褪色,证明原溶液中存在SO32-. |
①原理:SO32-+I2+H2O═SO42-+2I-+2H+
HSO3-+I2+H2O═SO42-+2I-+3H+
②步骤:准确量取10.00mL溶液于锥形瓶中,滴加几滴淀粉溶液,用0.1000mol/L碘液滴定至终点,消耗碘液20.00mL;再用0.2000mol/L NaOH溶液滴定生成的酸,消耗NaOH溶液23.00mL.
③计算:c(Na2SO3)=
考点:二氧化硫的化学性质,探究物质的组成或测量物质的含量
专题:氧族元素
分析:(1)根据发生装置、收集装置、尾气处理装置来排序,用Na2SO3粉末与浓H2SO4制备并收集SO2,需要固液混合不加热型装置,生成的二氧化硫密度大于空气,且常温下和空气不反应,所以采用向上排空气法收集,尾气处理中要防止倒吸;
(2)检验钠离子用焰色反应方法;检验氢氧根离子用酚酞试液,且要除去其它微粒干扰;检验亚硫酸根离子用酸化的品红溶液;
(3)根据滴定和中和消耗碘和氢氧化钠的量根据方程式计算.
(2)检验钠离子用焰色反应方法;检验氢氧根离子用酚酞试液,且要除去其它微粒干扰;检验亚硫酸根离子用酸化的品红溶液;
(3)根据滴定和中和消耗碘和氢氧化钠的量根据方程式计算.
解答:
解:(1)根据发生装置、收集装置、尾气处理装置来排序,用Na2SO3粉末与浓H2SO4制备并收集SO2,需要固液混合不加热型装置,生成的二氧化硫密度大于空气,且常温下和空气不反应,所以采用向上排空气法收集,尾气处理中要防止倒吸,所以其排列顺序是①④③⑤,故答案为:①④③⑤;
(2)步骤1预期现象和结论为:火焰呈黄色,证明原溶液中存在Na+.可知步骤1为检验钠离子,用焰色反应,具体操作为:用光洁无锈的铁丝蘸取原溶液在酒精灯火焰上灼烧;
步骤2预期现象和结论为:酚酞变为红色,证明原溶液中存在OH-.可知步骤2检验氢氧根离子,根据所给试剂,应先把亚硫酸钠除去,应亚硫酸钠水解显碱性,故先加过量氯化钙使亚硫酸钠生成亚硫酸钙沉淀,再用酚酞检验氢氧根离子,酚酞变红,证明含氢氧根离子;
故实验步骤为:取少量原溶液于试管中,加入过量CaCl2溶液,充分反应后静置,向上层清夜中滴加几滴酚酞,振荡;
步骤3预期现象和结论为:品红溶液褪色,证明原溶液中存在SO32-.说明步骤3检验亚硫酸钠,可把亚硫酸钠和盐酸反应生成二氧化硫,通过品红来检验,具体操作为:另取少量原溶液于试管中,滴入几滴品红溶液,再加入过量稀盐酸,振荡;
故答案为:
(3)设Na2SO3的物质的量为x,NaHSO3的物质的量为y,
SO32-+I2+H2O═SO42-+2I-+2H+
x x 2x
HSO3-+I2+H2O═SO42-+2I-+3H+
y y 3y
根据题意:
解得:x=0.0014,y=0.0006
c(Na2SO3)=
=0.1400mol/L,c(NaHSO3)=
=0.0600mol/L,
故答案为:0.1400;0.0600.
(2)步骤1预期现象和结论为:火焰呈黄色,证明原溶液中存在Na+.可知步骤1为检验钠离子,用焰色反应,具体操作为:用光洁无锈的铁丝蘸取原溶液在酒精灯火焰上灼烧;
步骤2预期现象和结论为:酚酞变为红色,证明原溶液中存在OH-.可知步骤2检验氢氧根离子,根据所给试剂,应先把亚硫酸钠除去,应亚硫酸钠水解显碱性,故先加过量氯化钙使亚硫酸钠生成亚硫酸钙沉淀,再用酚酞检验氢氧根离子,酚酞变红,证明含氢氧根离子;
故实验步骤为:取少量原溶液于试管中,加入过量CaCl2溶液,充分反应后静置,向上层清夜中滴加几滴酚酞,振荡;
步骤3预期现象和结论为:品红溶液褪色,证明原溶液中存在SO32-.说明步骤3检验亚硫酸钠,可把亚硫酸钠和盐酸反应生成二氧化硫,通过品红来检验,具体操作为:另取少量原溶液于试管中,滴入几滴品红溶液,再加入过量稀盐酸,振荡;
故答案为:
| 实验步骤 | 预期现象和结论 |
| 步骤1:用光洁无锈的铁丝蘸取原溶液在酒精灯火焰上灼烧 | 火焰呈黄色,证明原溶液中存在Na+. |
| 步骤2:取少量原溶液于试管中,加入过量CaCl2溶液,充分反应后静置,向上层清夜中滴加几滴酚酞,振荡 | 酚酞变为红色,证明原溶液中存在OH-. |
| 步骤3:另取少量原溶液于试管中,滴入几滴品红溶液,再加入过量稀盐酸,振荡 | 品红溶液褪色,证明原溶液中存在SO32-. |
SO32-+I2+H2O═SO42-+2I-+2H+
x x 2x
HSO3-+I2+H2O═SO42-+2I-+3H+
y y 3y
根据题意:
|
解得:x=0.0014,y=0.0006
c(Na2SO3)=
| 0.0014mol |
| 0.01L |
| 0.0006mol |
| 0.01L |
故答案为:0.1400;0.0600.
点评:本题以二氧化硫为载体考查物质含量测定、二氧化硫的制取和收集、实验方案设计等知识点,综合性较强,侧重考查学生分析、计算、实验设计能力,明确物质的性质及实验原理是解本题关键,难点是实验设计,要依据物质的性质、特殊现象设计实验,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于有机物的说法正确的是( )
| A、苯分子中既含碳碳单键,又含碳碳双键 |
| B、乙酸分子中存在共价键 |
| C、CH4和C3H8互为同分异构体 |
| D、纤维素、油脂、蛋白质都属于天然高分子化合物 |
HClO4、H2SO4、HCl和HNO3都是强酸,其酸性在水溶液中差别不大.以下是某温度下这四种酸在冰醋酸中的电离常数,下列说法正确的是( )
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | Ka1:6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A、温度对这四种酸在冰醋酸中的电离常数无影响 |
| B、在冰醋酸中HClO4是这四种酸中最强的酸 |
| C、在冰醋酸中H2SO4的电离方程式为H2SO4?2H++SO42- |
| D、这四种酸在冰醋酸中都没有完全电离,所以均属于弱电解质 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、CO2 |
| B、Cl2 |
| C、NaHCO3 |
| D、NaOH |
下列各组离子中,能在溶液中大量共存的是( )
| A、H+、Cl-、Na+、CO32- |
| B、Na+、Ag+、Cl-、NO3- |
| C、Cu2+、Mg2+、SO42-、Cl- |
| D、H+、Na+、Cl-、OH- |
下列四组离子中,不能在溶液中大量共存的是( )
| A、Na+、CO32-、Cl- |
| B、Ba2+、Na+、Cl- |
| C、H+、SO42-、OH- |
| D、Ag+、Al3+、NO3- |
下列有关钢铁腐蚀与防护的说法不正确的是( )
| A、生铁比纯铁容易生锈 |
| B、钢铁的腐蚀生成疏松氧化膜,不能保护内层金属 |
| C、钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-═4OH- |
| D、为保护地下钢管不受腐蚀,可使其与直流电源正极相连 |