题目内容
已知下列微粒在酸性溶液中还原性强弱的顺序是SO2>I->H2O2>Fe2+>Cl-,则下列反应不能发生的是( )
| A、2Fe2十+Cl2=2Fe3++2Cl- |
| B、2Fe2十+I2=2Fe3++2I- |
| C、I2+SO2+2H2O=H2SO4+2HI |
| D、H2O2+H2SO4=SO2↑+O2↑+2H2O |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:根据氧化还原反应的强弱规律,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物;在酸性溶液中还原性强弱的顺序是SO2>I->H2O2>Fe2+>Cl-,在溶液中进行的反应只能前面的粒子还原后面的,否则反应不能发生,据此对各选项进行解答.
解答:
解:A.2Fe2++Cl2=2Fe3++2Cl-反应中,还原剂Fe2+的还原性大于还原产物Cl-,符合题给条件,该反应可以发生,故A错误;
B.反应2Fe2++I2=2Fe3++2I-中,亚铁离子还原性大于I-,与题干信息不相符,该反应不能发生,故B正确;
C.I2+SO2+2H2O=H2SO4+2HI反应中,还原剂SO2的还原性大于还原产物Fe2+,该反应可以发生,故C错误;
D.H2O2+H2SO4=SO2↑+O2↑+2H2O,根据元素化合价可知,反应中硫元素化合价降低,过氧化氢中氧元素化合价升高,双氧水为还原剂,二氧化硫为还原产物,还原剂H2O2的还原性大于还原产物SO2,与题意不符,该反应不能发生,故D正确;
故选BD.
B.反应2Fe2++I2=2Fe3++2I-中,亚铁离子还原性大于I-,与题干信息不相符,该反应不能发生,故B正确;
C.I2+SO2+2H2O=H2SO4+2HI反应中,还原剂SO2的还原性大于还原产物Fe2+,该反应可以发生,故C错误;
D.H2O2+H2SO4=SO2↑+O2↑+2H2O,根据元素化合价可知,反应中硫元素化合价降低,过氧化氢中氧元素化合价升高,双氧水为还原剂,二氧化硫为还原产物,还原剂H2O2的还原性大于还原产物SO2,与题意不符,该反应不能发生,故D正确;
故选BD.
点评:本题考查了氧化还原反应的强弱规律的应用,题目难度中等,注意掌握氧化还原反应的特征及氧化性、还原性强弱大小的判断方法,明确溶液中进行的反应,必须满足:氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物.

练习册系列答案
相关题目
对于2KI+Br2=2KBr+I2和2HBrO3+I2=2HIO3+Br2两反应,下列叙述不正确的是( )
| A、Br2的氧化性强于I2氧化性 | ||||
| B、I-的还原性强于Br-的还原性 | ||||
| C、I2的氧化性强于Br2的氧化性 | ||||
D、BrO
|
能说明甲烷是正四面体形而非正方形平面结构的理由是( )
| A、其一氯取代物不存在同分异构体 |
| B、其二氯取代物不存在同分异构体 |
| C、它有四个C-H共价键 |
| D、它比较稳定,与强酸、强碱不反应 |
有8种物质:①甲烷;②苯;③聚乙烯;④邻二甲苯; ⑤乙炔; 既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A、③④⑤ | B、④⑤ |
| C、只有⑤ | D、全部 |
单质X能从盐溶液中转换出单质Y,由此可知( )
| A、当X、Y都是金属时,X不一定比Y活泼 |
| B、当X、Y都是非金属时,Y一定比X活泼 |
| C、当X是金属时,Y可能是金属也可能是非金属 |
| D、当X是非金属时,Y可能是金属也可能是非金属 |
用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图正确的是( )
A、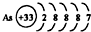 砷原子结构示意简图 |
B、 水合钠离子示意简图 |
C、 CO2分子示意图 |
D、 氧化还原反应与电子转移关系的示意图 |
下列实验操作或装置能达到实验目的是( )
A、 浓硫酸的稀释 |
B、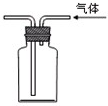 利用排空气法收集CO2 |
C、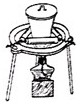 高温灼烧还带成灰 |
D、 制备氨气 |
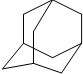 金刚烷(C10H16)是一种重要的脂肪烷烃,其结构高度对称,如图.金刚烷能与卤素发生取代反应,其中一氯一溴金刚烷(C10H14ClBr)的同分异构体数目是( )
金刚烷(C10H16)是一种重要的脂肪烷烃,其结构高度对称,如图.金刚烷能与卤素发生取代反应,其中一氯一溴金刚烷(C10H14ClBr)的同分异构体数目是( )