题目内容
8.设NA表示阿伏伽德罗常数,下列叙述中不正确的是( )| A. | 常温下,1.7g的OH-中所含的电子数为NA | |
| B. | 常温常压下,32g氧气和臭氧的混合气体中含氧原子的数目为2 NA | |
| C. | 标准状况下11.2LCO2与常温常压下8.5gNH3所含分子数相等 | |
| D. | 体积相同的两种气体,所含分子数目一定相同 |
分析 A.质量转化为物质的量,结合1个氢氧根离子含有10个电子解答;
B.氧气与臭氧都是由氧原子构成,依据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$计算解答;
C.依据n=$\frac{V}{Vm}$=$\frac{m}{M}$计算解答;
D.气体状况未知.
解答 解:A.常温下,1.7g的OH-中所含的电子数为$\frac{1.7g}{17g/mol}$×10×NA=NA,故A正确;
B.常温常压下,32g氧气和臭氧的混合气体中含氧原子的数目为$\frac{32g}{16g/mol}$×NA=2 NA,故B正确;
C.标准状况下11.2LCO2含有分子数为:$\frac{11.2L}{22.4L/mol}$×NA=0.5NA,常温常压下8.5gNH3所含分子数为:$\frac{8.5g}{17g/mol}$×NA=0.5NA,含有分子数相等,故C正确;
D.依据阿伏伽德罗定律:同温同压下相同体积的气体具有相同分子数,题干中温度压强未知,所以体积相同的两种气体,所含分子数目不一定相同,故D错误;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意阿伏伽德罗定律的条件.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
18.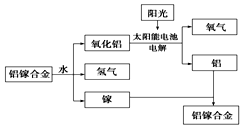 美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )
美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )
 美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )
美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )| A. | 铝镓合金与水反应的化学方程式为2Al+3H2O$\frac{\underline{\;一定条件\;}}{\;}$Al2O3+3H2↑ | |
| B. | 总反应式为2H2O$\frac{\underline{\;一定条件\;}}{\;}$2H2↑+O2↑ | |
| C. | 该过程中,能量的转化形式只有两种 | |
| D. | 铝镓合金可以循环使用 |
19.下列金属冶炼的反应原理正确的是( )
| A. | 2Al2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Al+3CO2↑ | B. | CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑ | ||
| C. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 | D. | 2HgO$\frac{\underline{\;电解\;}}{\;}$2Hg+O2↑ |
16. 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
| A. | 1 mol CH3OH完全燃烧放出192.9 kJ热量 | |
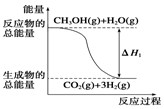
| B. | 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程不一定要吸收能量 | |
| D. | 根据②推知:CH3OH(1)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H<-192.9 kJ•mol-1 |
3.下列现象或新技术应用中,不涉及胶体性质的是( )
| A. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 | |
| B. | 使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血 | |
| C. | 江河入海口常形成三角洲 | |
| D. | 肾衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
20.按照冶金工业的分类,下列合金属于黑色金属材料的是( )
| A. | 锰钢 | B. | 青铜 | C. | 铝锂合金 | D. | 镧镍储氢合金 |
17.进行化学实验必须注意安全,下列说法正确的是( )
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将酸溅到眼中,应立即用烧碱溶液冲洗,边洗边眨眼睛 | |
| C. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上稀硫酸 | |
| D. | 配制稀硫酸,可先在量筒中加入一定体积的水,再边搅拌边慢慢加入浓硫酸 |
18.下列说法正确的是( )
| A. | 影响气体体积大小的主要因素为微粒数目与微粒间的距离 | |
| B. | 可利用MnO2和浓盐酸常温下反应制取氯气 | |
| C. | 相同温度下,在水中Na2CO3的溶解度小于NaHCO3 | |
| D. | 氧化还原反应的本质是存在元素化合价的升降 |