题目内容
4.在常温下,X2(g)和H2反应生成HX的平衡常数如表中所示,仅依据K的变化,关于等物质的量浓度的H2与X2的反应,下列说法正确的是( )| 化学方程式 | 平衡常数K | 化学方程式 | 平衡常数K |
| F2+H2?2HF | 6.5×1095 | Br2+H2?2HBr | 1.9×1019 |
| Cl2+H2?2HCl | 2.6×1033 | I2+H2?2HI | 8.7×102 |
| A. | X2与H2反应的反应速率依次减小 | B. | F2的转化率最大 | ||
| C. | X2与H2反应的剧烈程度逐渐减弱 | D. | 升高温度,平衡常数都增大 |
分析 A.反应速率与反应条件有关,题干中 无反应条件不能确定反应速率;
B.K值越大,说明反应的正向程度越大,即转化率越高;
C.反应的正向程度越小,说明生成物越不稳定,越易分解,反应程度越小,但不能判断与氢气反应的剧烈程度;
D.碘化氢不稳定易分解.
解答 解:A.反应速率受反应条件的影响,条件不定不能确定反应速率大小,故A错误;
B.K值越大,说明反应的正向程度越大,HF反应平衡常数最大,F2转化率最大,故B正确;
C.缺少反应条件,仅根据平衡常数,不能判断反应的剧烈程度,故C错误;
D.碘化氢不稳定易分解,升温碘化氢分解平衡常数减小,故D错误;
故选B.
点评 本题考查了影响影响化学反应速率、化学平衡、平衡常数的影响因素分析判断,注意反应速率、反应剧烈程度和反应条件有关,与平衡常数无直接关系,题目难度中等.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
15.下列物质既属于芳香烃,又属于苯的同系物的是( )
① ②
②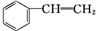 ③
③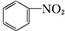 ④
④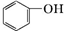 ⑤
⑤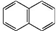
⑥
①
 ②
② ③
③ ④
④ ⑤
⑤
⑥

| A. | ③④ | B. | ①⑥ | C. | ①②⑤⑥ | D. | ②⑤ |
12.由于金属锌本身的价值不高,在我国工业锌废料的回收利用率比较低,某课题组研究利用含少量铜、铁的粗锌制备硫酸锌及相关物质的资源综合利用,其工艺流程图(图中加入的物质均为足量)及有关数据如下:
请回答下列问题:
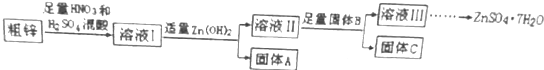
(1)固体A的主要成分是Fe(OH)3,加入固体B的主要作用是除去溶液Ⅱ中的Cu2+.
(2)粗锌中的铜与稀混酸溶液反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(3)若溶液Ⅱ中c(Cu2+)为0.05mol•L-1,则溶液Ⅱ的pH≤5.
(4)若B是Zn,取8.320gC完全溶解于500mL1mol•L-1稀硝酸中,共收集到2240mL气体,再向所得溶液中加入NaOH溶液至刚好生成沉淀最多,此时所得沉淀质量(m)的取值范围是13.42;若B是另一种物质,取部分C于试管中,加入盐酸后产生了有臭鸡蛋味气体,则该反应的离子方程式为ZnS+2H+=H2S↑+Zn2+.
请回答下列问题:

| 物质 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS |
| Ksp | 4.0×10-38 | 5.0×10-20 | 2.0×10-16 | 8.5×10-45 | 1.2×10-23 |
(2)粗锌中的铜与稀混酸溶液反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(3)若溶液Ⅱ中c(Cu2+)为0.05mol•L-1,则溶液Ⅱ的pH≤5.
(4)若B是Zn,取8.320gC完全溶解于500mL1mol•L-1稀硝酸中,共收集到2240mL气体,再向所得溶液中加入NaOH溶液至刚好生成沉淀最多,此时所得沉淀质量(m)的取值范围是13.42;若B是另一种物质,取部分C于试管中,加入盐酸后产生了有臭鸡蛋味气体,则该反应的离子方程式为ZnS+2H+=H2S↑+Zn2+.
19.下列性质能代表卤素通性的是( )
| A. | H2+X2═2HX | B. | X2+H20═HX+HXO | ||
| C. | NaX+AgNO3═AgX↓+NaNO3 | D. | 2NaX+H2SO4(浓)═Na2SO4+2HX |
9.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列说法正确的是( )
| A. | 在熔融电解质中,O2-向正极定向移动 | |
| B. | 电池的总反应是:2C4H10+13O2═8CO2+10H2O | |
| C. | 通入空气的一极是正极,电极反应为:O2+4e-+2H2O═4OH- | |
| D. | 通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-═4CO2↑+5H2O |
13.下列各项表述与示意图一致的是( )


| A. | 图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0;使用和未使用催化剂时,反应过程中的能量变化 | |
| B. | 图②表示25℃时,用0.01mol•L-1盐酸滴定一定体积的0.01mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | 图③表示CH4(g)+H2O(g)?CO(g)+3H2(g)△H,反应CH4的转化率与温度、压强的关系,且P1>P2、△H>0 | |
| D. | 图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0;正、逆反应的平衡常数K随温度的变化 |
14.下列氯的化合物中,不能由氯气与相应的金属反应制取的是( )
| A. | FeCl3 | B. | CuCl2 | C. | FeCl2 | D. | NaCl |
 X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
X、Y、Z、W四种短周期元素在周期表中的位置关系如图: ,工业合成该物质的化学方程式为N2+3H2$?_{催化剂}^{高温高压}$2NH3.
,工业合成该物质的化学方程式为N2+3H2$?_{催化剂}^{高温高压}$2NH3.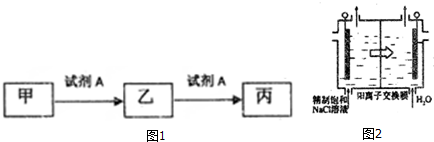
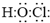 .二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠(NaClO3)和另一种氯的含氯酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-═ClO3-+ClO2-+H2O
.二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠(NaClO3)和另一种氯的含氯酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-═ClO3-+ClO2-+H2O