题目内容
将1.5mol Ba(OH)2溶液逐滴滴入明矾溶液中:①当OH-刚好将溶液中的Al3+沉淀时;②当全部Ba2+刚好将溶液中的SO42-沉淀时.两种情况下,生成沉淀的物质的量分别为( )
| A、2mol、3mol |
| B、2mol、1mol |
| C、1.5mol、1.5mol |
| D、2.5mol、1.5mol |
考点:化学方程式的有关计算
专题:计算题
分析:①当OH-刚好将溶液中的Al3+沉淀时,发生反应:2KAl(SO4)2+3Ba(OH)2=3BaSO4↓+2Al(OH)3↓+K2SO4;②当全部Ba2+刚好将溶液中的SO42-沉淀时,发生反应:KAl(SO4)2+2Ba(OH)2=2BaSO4↓+KAlO2+2H2O,根据方程式计算生成沉淀.
解答:
解:①当OH-刚好将溶液中的Al3+沉淀时,发生反应:2KAl(SO4)2+3Ba(OH)2=3BaSO4↓+2Al(OH)3↓+K2SO4,可知生成沉淀为1.5mol×
=2.5mol;
②当全部Ba2+刚好将溶液中的SO42-沉淀时,发生反应:KAl(SO4)2+2Ba(OH)2=2BaSO4↓+KAlO2+2H2O,可知生成沉淀为1.5mol,
故选D.
| 5 |
| 3 |
②当全部Ba2+刚好将溶液中的SO42-沉淀时,发生反应:KAl(SO4)2+2Ba(OH)2=2BaSO4↓+KAlO2+2H2O,可知生成沉淀为1.5mol,
故选D.
点评:本题考查化学方程式有关计算,难度中等,明确发生的反应是关键.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
在下列指定条件的溶液中,能大量共存的一组离子是( )
| A、pH=1的溶液中:NH4+、Fe2+、SO42-、ClO- |
| B、通入过量SO2气体后的溶液中:K+、Na+、CO32-、SO42- |
| C、AlO2一的浓度为0.1 mol/L的溶液中:K+、Na+、SiO32-、SO42- |
| D、常温下,由水电离出的c(H+)=1×10-11mol/L的溶液中:Fe3+、Br-、Cl-、SCN- |
下列有关说法正确的是( )
| A、油脂在酸性条件下水解可得高级脂肪酸和丙醇 |
| B、葡萄糖和蔗糖都含有C、H、O三种元素,但不是同系物 |
| C、可利用紫色石磊试液来鉴别苯、溴苯和乙醇 |
| D、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |
已知在室温时纯水中存在电离平衡:H2O?H++OH-.下列叙述正确的是( )
| A、同浓度、同体积的NaOH和氨水溶液中,水的电离程度相同 |
| B、升高温度,水的电离程度增大,c(H+)增大,pH<7,所以溶液显酸性 |
| C、向水中加入氨水,平衡逆向移动,水的电离受到抑制,所以c(OH-)降低 |
| D、向水中加入少量硫酸,c(H+)增大 |
在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为( )
| A、正十二面体 | B、正八面体 |
| C、正六面体 | D、正四面体 |
 将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如图,符合图中情况的一组物质是( )
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如图,符合图中情况的一组物质是( )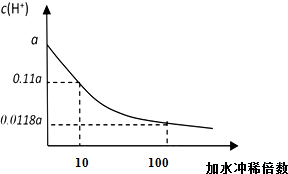 某HA的稀溶液,其浓度为b mol/L,在稀释过程中的c(H+)变化如图所示.
某HA的稀溶液,其浓度为b mol/L,在稀释过程中的c(H+)变化如图所示.