题目内容
实验室中可用如图1所示装置制取氯酸钾(KClO3),、次氯酸钠和探究氯水的性质.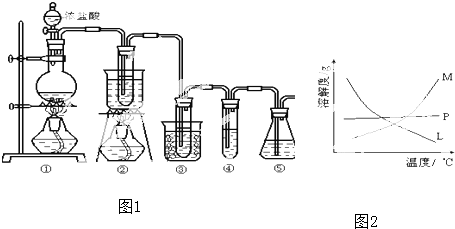
图1中:①为氯气发生装置;
②的试管里盛有15mL 30% KOH 溶液,并置于热水浴中;
③的试管里盛有15mL 8% NaOH 溶液,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
完成下列各题
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,再加入适量的浓盐酸,加热.实验时为除去氯气中的氯化氢气体,可在①与②之间安装盛有 (填写下列编号字母)的净化装置.
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是 .反应完毕经冷却后,②的试管中有大量晶体析出.图2中符合该晶体溶解度曲线的是 (填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验操作名称).
(3)本实验中制取次氯酸钠的离子方程式为 .
(4)实验中④的试管里溶液颜色先变红后褪色,解释溶液颜色变红的原因 .

图1中:①为氯气发生装置;
②的试管里盛有15mL 30% KOH 溶液,并置于热水浴中;
③的试管里盛有15mL 8% NaOH 溶液,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
完成下列各题
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,再加入适量的浓盐酸,加热.实验时为除去氯气中的氯化氢气体,可在①与②之间安装盛有
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
(3)本实验中制取次氯酸钠的离子方程式为
(4)实验中④的试管里溶液颜色先变红后褪色,解释溶液颜色变红的原因
考点:氯气的实验室制法,氯气的化学性质
专题:卤族元素
分析:(1)依据浓盐酸的挥发性,分析氯气含有的杂质,依据氯化氢易溶于水的性质解答;
(2)在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠;
溶质的溶解度随温度的降低而降低;
(3)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(4)依据氯气与水反应生成的产物的性质解答.
(2)在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠;
溶质的溶解度随温度的降低而降低;
(3)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(4)依据氯气与水反应生成的产物的性质解答.
解答:
解:(1)浓盐酸具有挥发性,制取的氯气中含有氯化氢气体,通过饱和食盐水可以吸收氯化氢气体,所以为除去氯气中的氯化氢气体,可在①与②之间安装盛有饱和食盐水的装置,
故答案为:B;
(2)根据题中信息可知,在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,二者反应的浓度和温度都不相同;
反应完毕经冷却后,②的试管中有大量晶体析出,说明溶质的溶解度随温度的降低而降低,只有M符合,不溶性固体与液体的分离常采用过滤的方法;
故答案为:制取温度不同,制取时碱的浓度也不同;M;过滤;
(3)氯气与氢氧化钠溶液反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(4)氯气与水反应生成氯化氢和次氯酸,氯化氢电离产生氢离子,溶液显酸性,所以紫色石蕊试液变红色;
故答案为:氯气与水反应生成氯化氢和次氯酸,氯化氢电离产生氢离子,溶液显酸性,所以紫色石蕊试液变红色.
故答案为:B;
(2)根据题中信息可知,在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,二者反应的浓度和温度都不相同;
反应完毕经冷却后,②的试管中有大量晶体析出,说明溶质的溶解度随温度的降低而降低,只有M符合,不溶性固体与液体的分离常采用过滤的方法;
故答案为:制取温度不同,制取时碱的浓度也不同;M;过滤;
(3)氯气与氢氧化钠溶液反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(4)氯气与水反应生成氯化氢和次氯酸,氯化氢电离产生氢离子,溶液显酸性,所以紫色石蕊试液变红色;
故答案为:氯气与水反应生成氯化氢和次氯酸,氯化氢电离产生氢离子,溶液显酸性,所以紫色石蕊试液变红色.
点评:本题考查实验方案的设计,熟悉氯气的制取原理及物质的性质是解答本题的关键,题目难度中等.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
根据你的生活经验和所学的科学知识,判断下列做法正确的是( )
| A、用钢丝球洗涮铝锅 |
| B、用活性炭除去冰箱里的异味 |
| C、室内烤火放一盆水,防止CO中毒 |
| D、用水浇灭着火的油锅 |
如图是元素周期表的一部分,下列说法中正确的是( )
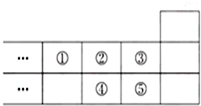

| A、5种元素的单质中,①单质的熔、沸点最高 |
| B、气态氢化物的稳定性:④>② |
| C、最高价氧化物对应水化物酸性:⑤>④ |
| D、元素的最高正化合价:③=⑤ |
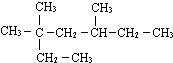
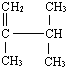
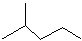 表示的分子式
表示的分子式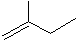 表示的分子式是
表示的分子式是