题目内容
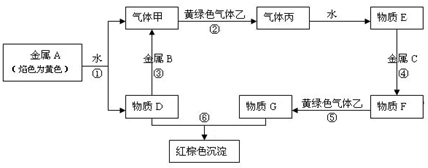
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).请根据以上信息回答下列问题:
(1)写出金属元素A的原子结构示意图: .
(2)写出下列反应的离子方程式:
反应③ ;
反应⑤
(3)在F的水溶液中滴加D的溶液将会观察到 .
(4)请写出实验室制取黄绿色气体乙的化学方程式 ,在该反应中如有0.5mol乙生成,转移的电子的物质的量是 mol.制取完毕,多余的乙将用D的水溶液来吸收,其离子方程式为 .

(1)写出金属元素A的原子结构示意图:
(2)写出下列反应的离子方程式:
反应③
反应⑤
(3)在F的水溶液中滴加D的溶液将会观察到
(4)请写出实验室制取黄绿色气体乙的化学方程式
考点:无机物的推断
专题:推断题
分析:金属A焰色反应为黄色,故A为金属Na,由反应①可知,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,故金属B为Al.黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸.氢氧化钠与物质G反应生成红褐色沉淀是Fe(OH)3,故物质G中含有Fe3+,由转化关系HCl
物质F
物质G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3,据此答题.
| 金属C |
| 氯气 |
解答:
解:金属A焰色反应为黄色,故A为金属Na,由反应①可知,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,故金属B为Al.黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸.氢氧化钠与物质G反应生成红褐色沉淀是Fe(OH)3,故物质G中含有Fe3+,由转化关系HCl
物质F
物质G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3,
(1)根据上面的分析可知,A为金属Na,A的原子结构示意图为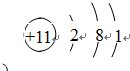 ,
,
故答案为: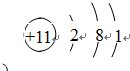 ;
;
(2)反应③是Al与NaOH溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;反应⑤氯化亚铁与氯气反应生成氯化铁,反应离子方程式为:2Fe2++Cl2═2Fe3++2Cl-;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;2Fe2++Cl2═2Fe3++2Cl-;
(3)F为FeCl2,D为NaOH,在F的水溶液中滴加D的溶液将会观察到先生成白色絮状沉淀,为氢氧化亚铁,沉淀迅速转变成灰绿色,最后转变成红褐色的氢氧化铁,
故答案为:先生成白色絮状沉淀,沉淀迅速转变成灰绿色,最后转变成红褐色;
(4)实验室用二氧化锰与浓盐酸加热制取氯气,反应的化学方程式为MnO2+4HCl
MnCl2+Cl2↑+2H2O,根据化学方程式可知,每生成1mol氯气可转移2mol电子,所以如有0.5mol氯气生成,转移的电子的物质的量是1 mol.制取完毕,多余的氯气用氢氧化钠溶液来吸收,其离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:MnO2+4HCl
MnCl2+Cl2↑+2H2O;1;Cl2+2OH-=Cl-+ClO-+H2O;
| 金属C |
| 氯气 |
(1)根据上面的分析可知,A为金属Na,A的原子结构示意图为
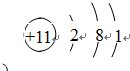 ,
,故答案为:
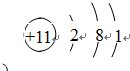 ;
;(2)反应③是Al与NaOH溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;反应⑤氯化亚铁与氯气反应生成氯化铁,反应离子方程式为:2Fe2++Cl2═2Fe3++2Cl-;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;2Fe2++Cl2═2Fe3++2Cl-;
(3)F为FeCl2,D为NaOH,在F的水溶液中滴加D的溶液将会观察到先生成白色絮状沉淀,为氢氧化亚铁,沉淀迅速转变成灰绿色,最后转变成红褐色的氢氧化铁,
故答案为:先生成白色絮状沉淀,沉淀迅速转变成灰绿色,最后转变成红褐色;
(4)实验室用二氧化锰与浓盐酸加热制取氯气,反应的化学方程式为MnO2+4HCl
| ||
故答案为:MnO2+4HCl
| ||
点评:本题是考查物质推断与性质、常用化学用语,难度中等,掌握元素化合物的性质是解题的关键,需要学生熟练掌握元素化合物知识,注意特殊的颜色与特殊反应是推断的突破口.

练习册系列答案
相关题目
下列各项中,含氧原子数不同的是( )
| A、质量比为2:1的SO2和O2 |
| B、9g水和23g乙醇(C2H5OH) |
| C、标准状况下44.8L的一氧化氮和100 ml 5mol/L的硫酸溶液 |
| D、物质的量相同的Na2SO4和FeSO4 |
下列玻璃仪器:①量筒②烧瓶 ③试管 ④容量瓶 ⑤烧杯.能直接加热的是( )
| A、①③ | B、③ | C、②③ | D、④⑤ |
石英光导纤维的主要成分是( )
| A、Si |
| B、SiC |
| C、SiO2 |
| D、Na2SiO3 |
下列各组离子在指定环境中一定能大量共存的是( )
| A、在碳酸氢钠溶液中:K+、Al3+、SO42-、Cl- |
| B、存在较多Fe3+的溶液中:Na+、SCN-、CO32-、K+ |
| C、常温下由水电离出的C(H+)水?C(OH-)水=10-24溶液中:NH4+、Cl-、CO32-、F- |
| D、在能使pH试纸变深蓝色的溶液中:Na+、S2-、CO32-、NO3- |
设NA为阿伏伽德罗常数的值,下列叙述错误的是( )
| A、通常情况下,87g丙酮分子中含有的π键键数为1.5NA |
| B、标准状况下,11.2 L三氯甲烷分子中含有的σ键键数为2NA |
| C、2.5 mol乙醛与足量的氢气完全加成,断裂的π键键数为2.5NA |
| D、15 g 氨基乙酸通过成肽反应全部生成二肽时,生成的肽键键数为0.1NA |