题目内容
19.除去下表内各物质中含有的少量杂质,写出除杂试剂,并填写分离方法.| 序号 | 物质 | 杂质 | 所加试剂 | 分离方法 |
| (1) | NO | NO2 | ||
| (2) | Fe粉 | Al粉 | ||
| (3) | 氯化钠固体 | 氯化铵固体 | / |
分析 (1)NO2能和水反应生成NO;
(2)Al既能和酸反应又能和碱反应,而Fe只能和酸反应;
(3)氯化铵受热易分解.
解答 解:(1)NO2能和水反应生成NO,故可以用水洗气以除去NO中的NO2;
(2)Al既能和酸反应又能和碱反应,而Fe只能和酸反应,故可以用氢氧化钠溶液除去铁中的铝;
(3)氯化钠受热不分解,而氯化铵受热易分解,故可以用加热的方法来除去氯化钠中的氯化铵.
故答案为:
| 序号 | 物质 | 杂质 | 所加试剂 | 分离方法 |
| (1) | NO | NO2 | H2O | 洗气 |
| (2) | Fe粉 | Al粉 | NaOH溶液 | 过滤 |
| (3) | 氯化钠固体 | 氯化铵固体 | 加热 |
点评 本题考查了物质的除杂,应根据主体物质和杂质性质的不同来分析除杂方法,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A. | 2H2(g)+O2(g)═2H2O(g)△H1 2H2(g)+O2(g)═2H2O(l)△H2 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | 2HCl(g)═H2(g)+Cl2(g)△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H2 |
7.下列颜色变化过程中无化学反应发生的是( )
| A. | 蛋白质遇浓硝酸变黄 | |
| B. | 含钠元素的物质在火焰上灼烧产生黄色火焰 | |
| C. | pH试纸与某溶液接触变为红色 | |
| D. | 无色浓硝酸久置后变黄 |
14.实验中的下列操作正确的是( )
| A. | 将试剂瓶中的Na2CO3溶液倒入试管,发现取量过多,将过量的试剂倒回试剂瓶中 | |
| B. | 将含有Ba(NO3)2的废液倒入指定的容器中回收 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,立刻转移到容量瓶中 |
4.自然界中含量最多的金属元素是( )
| A. | Si | B. | Fe | C. | Cu | D. | Al |
11.下列有关说法不正确的是( )
| A. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 | |
| B. | 金属阳离子被还原不一定得到金属单质 | |
| C. | 铝在纯氧气中能剧烈燃烧,火星四射,生成熔融的氧化铝 | |
| D. | 生铁、普通钢和不锈钢中的含碳量依次降低 |
8.将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中缓慢逐滴加入浓度为 0.1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )
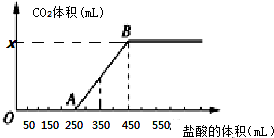

| A. | OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3- | |
| B. | 当加入350 mL盐酸时,产生CO2的体积为224 mL(标准状况) | |
| C. | x点对应的数值是448 | |
| D. | 混合物中NaOH的质量为1克 |
9.下列试剂保存方法或实验方法不正确的是( )
| A. | 盛浓硝酸、硝酸银用棕色试剂瓶,并置于阴凉处 | |
| B. | 用带玻璃塞的磨口玻璃瓶盛氢氧化钠 | |
| C. | 金属钠通常保存在煤油里 | |
| D. | HF酸储存在塑料瓶中 |