题目内容
11.80°C,0.1mol/L NaHB溶液中c(H+)>c(OH-),可能正确的关系是( )| A. | c(Na+)+c(H+)=c(HB-)+2c(B2-) | B. | 溶液的pH=1 | ||
| C. | c(H+)?c(OH-)=10-14 | D. | c(Na+)=c(H2B)+c(HB-) |
分析 0.1mol•L-1的NaHB溶液中c(H+)>c(OH-),说明HB-电离程度大于水解程度,溶液呈酸性,结合电荷守恒c(Na+)+c(H+)=c(HB-)+2c(B2-)+c(OH-)和物料守恒c(Na+)=c(B2-)+c(HB-)+c(H2B)解答该题;注意温度为80C.
解答 解:A.溶液存在电荷守恒:c(Na+)+c(H+)=c(HB-)+2c(B2-)+c(OH-),故A错误;
B.HB-若完全电离,则溶液的pH可能为1,故B正确;
C.常温下,水的离子积常数K=c(H+)•c(OH-)=10-14,80°C水的离子积增大,则c(H+)•c(OH-)>10-14,故C错误;
D.由物料守恒可知c(Na+)=c(B2-)+c(HB-)+c(H2B),故D错误;
故选B.
点评 本题考查离子浓度的大小比较,题目难度增大,注意题给信息的含义及应用,注意掌握电荷守恒和物料守恒的含义,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列化学方程式的书写正确的是( )
| A. | 硝酸见光分解:4HNO3$\frac{\underline{\;光照\;}}{\;}$4NO2↑+O2↑+2H2O | |
| B. | 往NaOH溶液中通入过量二氧化硫:2NaOH+SO2═Na2SO3+H2O | |
| C. | SO2气体通入BaCl2溶液中产生白色沉淀:SO2+BaCl2+H2O═BaSO3↓+2HCl | |
| D. | Fe与稀H2SO4反应的化学方程式为:2Fe+3H2SO4═Fe2(SO4)3+3H2↑ |
2.下列各组化合物中,化学键类型完全相同的是( )
| A. | Na2O2 和Na2O | B. | MgCl2 和Na2S | C. | CaO和CO2 | D. | HCl 和NaOH |
19.化学在生产和生活中有着重要的应用.下列说法不正确的是( )
| A. | 炼铁时增大高炉的高度,能有效减少CO的排放 | |
| B. | 明矾在水处理中可作净水剂 | |
| C. | 热电厂进行燃煤时将煤块压碎以提高煤的燃烧效率 | |
| D. | 在海轮外壳上镶嵌锌块,能减缓船体的腐蚀速率 |
6.下列反应的产物中,只存在+3价铁元素或氮元素的是( )
| A. | 过量的铁丝在氯气燃烧 | B. | 过量的铁粉与溴水反应 | ||
| C. | 烧碱溶液吸收NO2 | D. | 硝酸铜受热分解 |
16.有两份组成及质量都相等的Na2O2和Na2CO3的混合物,向第一份中加入足量的稀硫酸,放出的气体共4.48L.将此气体通入第二份混合物,充分反应后,气体体积变为4.032L(均为标准状况下体积).则原混合物中Na2O2和Na2CO3的物质的量之比为( )
| A. | 2:9 | B. | 3:2 | C. | 2:1 | D. | 8:1 |
3.下列化学用语书写正确的是( )
| A. | 四氯化碳的电子式: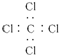 | B. | 乙醇的结构简式C2H6O | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 乙炔的结构式H-C≡C-H |
20.下列关于物质的用途,叙述不正确的是( )
| A. | 过氧化钠可用作供氧剂 | B. | 三氧化二铁可用做漆料 | ||
| C. | 镁铝合金可用作制造飞机的材料 | D. | 高纯硅用来制造光导纤维 |
1.下列说法不正确的是( )
| A. | 核磁共振氢谱不能区分CH3CH2OH和CH3OCH3 | |
| B. | 用溴水可以鉴别苯酚溶液、2,4-己二烯和甲苯 | |
| C. | 室温下,在水中的溶解度:甘油>苯酚>溴乙烷 | |
| D. | 两种二肽互为同分异构体,二者的水解产物可能相同 |