题目内容
(氢氧燃料电池)电解质溶液是KOH溶液(碱性电解质).负极: 正极: 总反应式: .
考点:电极反应和电池反应方程式
专题:
分析:氢氧燃料电池工作时,通入氢气的一极为电池的负极,发生氧化反应,通入氧气的一极为电池的正极,发生还原反应,电子由负极经外电路流向正极,电池总反应与氢气在氧气中燃烧的化学方程式一致,产物为水.
解答:
解:氢氧燃料电池工作时,通入氢气的一极为电池的负极,发生氧化反应,通入氧气的一极为电池的正极,发生还原反应.电解质溶液为KOH溶液时,
负极:氢气失电子和氢氧根离子反应生成水,电极反应式为H2+2OH--2e-=2H2O,即2H2+4OH--4e-=4H2O,
正极:氧气得电子和水生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,
总反应为:2H2+O2═2H2O,
故答案为:2H2+4OH--4e-=4H2O;O2+4e-+2H2O=4OH-;2H2+O2═2H2O.
负极:氢气失电子和氢氧根离子反应生成水,电极反应式为H2+2OH--2e-=2H2O,即2H2+4OH--4e-=4H2O,
正极:氧气得电子和水生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,
总反应为:2H2+O2═2H2O,
故答案为:2H2+4OH--4e-=4H2O;O2+4e-+2H2O=4OH-;2H2+O2═2H2O.
点评:本题考查考查原电池的工作原理,侧重电极反应式的书写,注意电解质溶液酸碱性对电极反应式的影响,书写电极反应式一定要结合电解质溶液酸碱性,为易错点,题目难度不大.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
在溶液中能大量共存,加入OH-有沉淀析出,加入H+有气体放出的是( )
| A、Mg2+、Na+、Cl-、CO32- |
| B、Fe3+、K+、SO42-、NO3- |
| C、H+、Al3+、OH-、NO3- |
| D、Na+、Ca2+、Cl-、HCO3- |
关于从碘水中分离出碘单质的实验,下列说法正确的是( )
| A、可以用酒精萃取出碘单质 |
| B、可以用CCl4萃取出碘单质,理由是CCl4密度比水大 |
| C、若用CCl4萃取出碘单质,萃取后下层液体呈紫红色 |
| D、若用CCl4萃取出碘单质,萃取后无色液体层应从分液漏斗的上口倒出 |
有机物A结构如图所示,下列说法正确的是( )
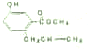

| A、A在碱性条件下不能发生水解反应 |
| B、1molA能和4mol氢气发生加成反应 |
| C、和溴水反应时,1molA能消耗1molBr2 |
| D、A不能使酸性高锰酸钾溶液褪色 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、0.1mol?L-1的NaF溶液中所含F-的数目小于0.1NA |
| B、标准情况下,2.24L乙醇中含有的C-H键数目为0.5NA |
| C、0.1mol Na完全被氧化生成Na2O2,转移电子的数目为NA |
| D、0.1mol O2中含氧原子数目为0.2NA |
1.0molPCl5充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl5(g)?PCl3(g)+Cl2(g)达平衡时,PCl3(g) 为0.4mol,如果此时再加入1.0molPCl5(g),在相同条件下再达到平衡时,下列说法正确的是( )
| A、PCl5为0.6mol |
| B、PCl3大于0.8mol |
| C、再次达平衡时PCl5的体积分数比原平衡减小 |
| D、再次达平衡时PCl5的转化率比原平衡减小 |

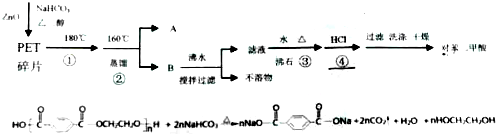
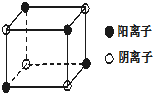 现有部分前四周期7种元素,原子序数依次增大,它们的性质或原子结构如下表:
现有部分前四周期7种元素,原子序数依次增大,它们的性质或原子结构如下表: