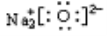题目内容
下列能说明氯元素比硫元素非金属性强的是
①HCl比H2S稳定;
②HClO4酸性比H2SO4强;
③Cl2能与H2S反应生成S;
④Cl原子最外层有7个电子,S原子最外层有6个电子;
⑤Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS;
⑥盐酸是强酸,而氢硫酸是弱酸
A.①②③④⑤⑥ B.①②③④⑥ C.①②③⑤ D.②④⑥
C
【解析】
试题分析:①利用气态氢化物的稳定性比较非金属性的强弱,正确;②利用最高价含氧酸的酸性的强弱,比较非金属性的强弱,正确;③利用单质之间的置换反应比较非金属性的强弱,正确;④最外层电子数目的多少不能判断非金属性的强弱,错误;⑤与同种单质反应,生成物中元素化合价的不同,可以判断非金属性的强弱,正确;⑥氢化物的水溶液的酸性不能比较非金属性的强弱,错误,答案选C。
考点:考查非金属性强弱判断的依据

练习册系列答案
相关题目
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )
元素代号 | A | B | D | E | G | I | J | K |
化合价 | –1 | –2 | +4 –4 | –1 | +5 –3 | +3 | +2 | +1 |
原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
A.A的单质能将E单质从KE的溶液中置换出来
B.A、I、J的离子半径由大到小顺序是A>J>I
C.G元素的单质不存在同素异形体
D.J在DB2中燃烧生成两种化合物
 图中单质可能为( )
图中单质可能为( )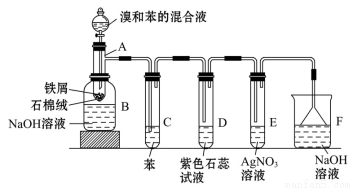
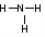 B.CO2分子模型的示意图:
B.CO2分子模型的示意图: