题目内容
15.X、Y、Z、R是短周期主族元素,X元素是形成有机化合物的必需元素,Y元素的原子最外层电子数是次外层的三倍,Z元素的原子半径是短周期元素中最大的,R原子的核外电子数是X原子核Z原子的核外电子数之和.下列叙述不正确的是( )| A. | XY2是形成酸雨的主要污染物 | |
| B. | X、Y、R三种元素的非金属性Y>R>X | |
| C. | X、Z分别与R形成的化合物中化学键类型不同 | |
| D. | 含有Y、Z、R三种元素的化合物溶液可能显碱性 |
分析 X元素是形成有机化合物的必需元素,应为C元素,Y元素的原子最外层电子数是次外层的三倍,应为O元素,Z元素的原子半径是短周期元素中最大的,为Na元素,R原子的核外电子数是X原子核Z原子的核外电子数之和,为Cl元素,结合对应单质、化合物的性质以及元素周期率知识解答该题.
解答 解:由以上分析可知X为C元素、Y为O元素、Z为Na元素、R为Cl元素.
A.二氧化碳为导致温室效应的主要气体,与酸雨无关,故A错误;
B.同周期元素O>C,由水比HCl稳定可知非金属性O>Cl,由酸性强弱可知Cl>C,故非金属性Y>R>X,故B正确;
C.X、Z分别与R形成的化合物分别为四氯化碳、氯化钠,分别含有共价键、离子键,故C正确;
D.如为NaClO,为强碱弱酸盐,溶液呈碱性,故D正确.
故选A.
点评 本题考查了元素的位置、结构和性质,为高考常见题型和高频考点,侧重考查学生的分析能力,正确推断元素是解本题关键,结合元素周期律来分析解答,易错选项是B,总结含有O、Cl的非金属性,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.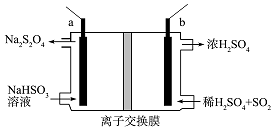 连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂.工业常用惰性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理装置如图所示,下列说法正确的是( )
连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂.工业常用惰性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理装置如图所示,下列说法正确的是( )
 连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂.工业常用惰性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理装置如图所示,下列说法正确的是( )
连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂.工业常用惰性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理装置如图所示,下列说法正确的是( )| A. | b电极应该接电源的负极 | |
| B. | 装置中所用离子交换膜为阴离子交换膜 | |
| C. | 电路中每转移1mole-消耗SO2的体积为11.2L | |
| D. | a电极的电极反应式为:2HSO3-+2e-+2H+═S2O42-+2H2O |
7.已知25℃时,CH3COOH和HCN的电离平衡常数分别为1.75×10-5、4.9×10-10,下列有关叙述正确的是( )
| A. | 中和等体积、等pH的CH3COOH溶液和HCN溶液消耗NaOH的量前者小于后者 | |
| B. | 常温下,等浓度CH3COONa溶液的pH大于NaCN溶液的pH | |
| C. | 常温下,等体积、等浓度CH3COONa溶液的离子总数等于NaCN溶液的离子总数 | |
| D. | 反应CH3COOH+CN-?HCN+CH3COO-的化学平衡常数为2.8×10-5 |
4.设NA为阿伏伽德罗常数.下列叙述中正确的是( )
| A. | 0.25mol Na2O2中含有的阴离子数为0.5NA | |
| B. | 等物质的量的OH-与烃基(-OH)所含电子数相等 | |
| C. | 惰性电极电解食盐水,若电路中通过NA个电子,则标况下阳极产生气体11.2L | |
| D. | 25℃时,pH=13的1.0LBa(OH)2溶液中含OH-数目为0.2NA |
10.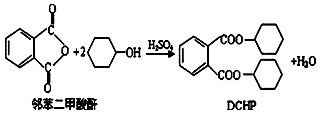 塑化剂是一种对人体有害的物质,增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得.下列说法正确的是( )
塑化剂是一种对人体有害的物质,增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得.下列说法正确的是( )
 塑化剂是一种对人体有害的物质,增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得.下列说法正确的是( )
塑化剂是一种对人体有害的物质,增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得.下列说法正确的是( )| A. | 环己醇能与溴水发生取代反应 | |
| B. | 1molDCHP可与2molNaOH完全反应 | |
| C. | DCHP与邻苯二甲酸酐均含有酯基,所以它们互为同系物 | |
| D. | DCHP易溶于水 |
19.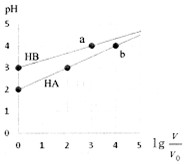 室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )
室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )
 室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )
室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )| A. | HA为强酸,HB为弱酸 | |
| B. | 水的电离程度a点大于b点 | |
| C. | 当pH=2时,HA溶液中$\frac{c(HA)}{c({A}^{-})}$=9 | |
| D. | 等浓度等体积的HB与Na0H溶液充分反应后,离子浓度关系大小为:c(B-)>c(Na+)>c(H+)>c(OH-) |
6.用NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A. | 22.4L氯气与足量镁粉充分反应后,转移的电子数为2NA | |
| B. | 常温下,1L0.5mo1•L-1 FeCl3溶液中含有的Fe3+数目一定小于0.5NA | |
| C. | 12g石墨中含有C-C共价键数为1.5NA | |
| D. | 28g由乙烯和环丁烷(C4H8)组成的混合气体中含有的碳原子数为2NA |
3.根据下列结构示意图,判断下列说法中正确的是( )

| A. | 在NaCl晶体中,距Na+最近的多个Cl-构成正四面体 | |
| B. | 在CaF2晶体中,每个晶胞平均占有4个Ca2+ | |
| C. | 在金刚石晶体中,碳原子与碳碳键数之比为1:2 | |
| D. | 该气态团簇分子的分子式为EH或HE |