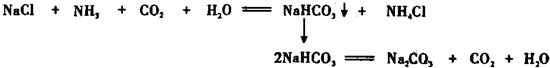题目内容
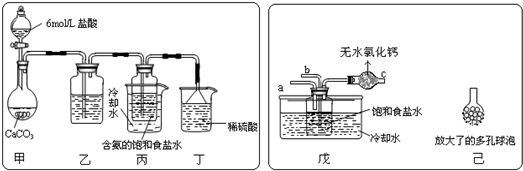
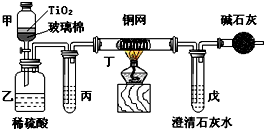 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol?L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.回答下列问题:
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol?L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.回答下列问题:(1)乙中反应的离子方程式为
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果.则丙中加入的除杂试剂是
a.饱和食盐水 b.饱和NaHCO3溶液 c.浓NaOH溶液 d.浓硫酸
(3)丁在实验中的作用是
(4)戊中盛有含Ca(OH)2 0.02mol的石灰水,若实验中戊中共生成0.82g沉淀,则该实验中测得CN-被处理的百分率等于
(5)请提出一个能提高准确度的建议(要有可操作性,不宜使操作变得过于复杂)
考点:性质实验方案的设计
专题:实验设计题
分析:(1)根据题意可知,乙中的反应为酸性条件下CNO-与NaClO反应生成N2、CO2和Cl2.根据氧化还原反应配平;
(2)丙中饱和食盐水除去混合气体中的氯化氢气体;
(3)铜网用来除去氯气,碱石灰作用是防止空气中的二氧化碳进入澄清石灰水反应;
(4)根据碳原子守恒,计算出被处理的CN-的物质的量,再利用200mL(其中CN-的浓度0.05mol/L)求出CN-被处理的百分率;装置中残留有CO2未被完全吸收,导致测定的二氧化碳质量偏低;
(5)能提高准确度的建议有:控制CO2的产生速度,使装置中滞留的CO2尽可能多到与Ca(OH)2反应,将戊中澄清石灰水改为浓度较大到NaOH溶液,反应结束后戊中加入足量CaCl2后测沉淀质量等方面分析.
(2)丙中饱和食盐水除去混合气体中的氯化氢气体;
(3)铜网用来除去氯气,碱石灰作用是防止空气中的二氧化碳进入澄清石灰水反应;
(4)根据碳原子守恒,计算出被处理的CN-的物质的量,再利用200mL(其中CN-的浓度0.05mol/L)求出CN-被处理的百分率;装置中残留有CO2未被完全吸收,导致测定的二氧化碳质量偏低;
(5)能提高准确度的建议有:控制CO2的产生速度,使装置中滞留的CO2尽可能多到与Ca(OH)2反应,将戊中澄清石灰水改为浓度较大到NaOH溶液,反应结束后戊中加入足量CaCl2后测沉淀质量等方面分析.
解答:
解:(1)根据题意可知,乙中的反应为酸性条件下CNO-与NaClO反应生成N2、CO2,反应离子方程式为2CNO-+2H++3ClO-=N2↑+2CO2↑+3Cl-+H2O,
故答案为:2CNO-+2H++3ClO-=N2↑+2CO2↑+3Cl-+H2O;
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,丙中饱和食盐水能够除去氯化氢杂质;丁中铜网能够和氯气反应从而除去氯气杂质;避免空气中的二氧化碳进入戊装置造成测定数据的干扰,用碱石灰吸收二氧化碳,
故答案为:a;
(3)丁中铜网能够和氯气反应从而除去氯气杂质;避免空气中的二氧化碳进入戊装置造成测定数据的干扰,用碱石灰吸收二氧化碳,
故答案为:去除Cl2;防止空气中CO2进入戊中影响测定准确度;
(4)200mL(其中CN-的浓度0.05mol/L)混合液中含有的CN-的物质的量是:0.2L×0.05mol/L=0.01mol,根据碳原子守恒,增多生成0.01mol二氧化碳,所以石灰水过量,生成的碳酸钙的物质的量是:0.0082mol,反应的CN-的物质的量是0.0082mol,CN-被处理的百分率是:
×100%=82%;
装置乙、丙、丁中可能滞留有CO2,未被完全吸收,导致测定的二氧化碳质量偏低,测得的CN-被处理的百分率与实际值相比偏低,
故答案为:82%;偏低;装置中残留有CO2未被完全吸收;
(5)能提高准确度的建议有:建议一:不将甲中溶液一次全部加入乙中,改为分次加入,控制CO2的产生速度;
建议二:乙中瓶塞改为三孔塞,增加丁那个孔中插入一根导管到液面以下,反应结束后缓缓通入除去CO2的空气,使装置中滞留的CO2尽可能多到与Ca(OH)2反应.
建议三:将戊中澄清石灰水改为浓度较大到NaOH溶液,反应结束后戊中加入足量CaCl2后测沉淀质量等,
故答案为:建议一、不将甲中溶液一次全部加入乙中,改为分次加入,控制CO2的产生速度;建议二、乙中瓶塞改为三孔塞,增加的那个孔中插入一根导管到液面以下,反应结束后缓缓通入除去CO2的空气,使装置中滞留的CO2尽可能多的与Ca(OH)2反应.建议三、将戊中澄清石灰水改为浓度较大的NaOH溶液,反应结束后向戊中加入足量CaCl2后测沉淀质量.
故答案为:2CNO-+2H++3ClO-=N2↑+2CO2↑+3Cl-+H2O;
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,丙中饱和食盐水能够除去氯化氢杂质;丁中铜网能够和氯气反应从而除去氯气杂质;避免空气中的二氧化碳进入戊装置造成测定数据的干扰,用碱石灰吸收二氧化碳,
故答案为:a;
(3)丁中铜网能够和氯气反应从而除去氯气杂质;避免空气中的二氧化碳进入戊装置造成测定数据的干扰,用碱石灰吸收二氧化碳,
故答案为:去除Cl2;防止空气中CO2进入戊中影响测定准确度;
(4)200mL(其中CN-的浓度0.05mol/L)混合液中含有的CN-的物质的量是:0.2L×0.05mol/L=0.01mol,根据碳原子守恒,增多生成0.01mol二氧化碳,所以石灰水过量,生成的碳酸钙的物质的量是:0.0082mol,反应的CN-的物质的量是0.0082mol,CN-被处理的百分率是:
| 0.0082mol |
| 0.01mol |
装置乙、丙、丁中可能滞留有CO2,未被完全吸收,导致测定的二氧化碳质量偏低,测得的CN-被处理的百分率与实际值相比偏低,
故答案为:82%;偏低;装置中残留有CO2未被完全吸收;
(5)能提高准确度的建议有:建议一:不将甲中溶液一次全部加入乙中,改为分次加入,控制CO2的产生速度;
建议二:乙中瓶塞改为三孔塞,增加丁那个孔中插入一根导管到液面以下,反应结束后缓缓通入除去CO2的空气,使装置中滞留的CO2尽可能多到与Ca(OH)2反应.
建议三:将戊中澄清石灰水改为浓度较大到NaOH溶液,反应结束后戊中加入足量CaCl2后测沉淀质量等,
故答案为:建议一、不将甲中溶液一次全部加入乙中,改为分次加入,控制CO2的产生速度;建议二、乙中瓶塞改为三孔塞,增加的那个孔中插入一根导管到液面以下,反应结束后缓缓通入除去CO2的空气,使装置中滞留的CO2尽可能多的与Ca(OH)2反应.建议三、将戊中澄清石灰水改为浓度较大的NaOH溶液,反应结束后向戊中加入足量CaCl2后测沉淀质量.
点评:本题考查了电镀后的废水中CN-离子的含量测定,该题是高考中的常见题型,属于中等难度的试题,试题综合性强,侧重对学生能力的培养和训练,有利于培养学生规范严谨的实验设计、操作能力.

练习册系列答案
相关题目
下列关于物质的量、摩尔质量的叙述正确的是( )
| A、氢氧化钠的摩尔质量是40g |
| B、1molH2O中含有2mol氢和1mol氧 |
| C、0.012 kg12C中含有约6.02×1023个碳原子 |
| D、2mol水的摩尔质量是1mol水的摩尔质量的2倍 |
下列物质与其用途相符合的是( )
①ClO2-消毒剂
②NaHCO3-治疗胃酸过多
③明矾-做干燥剂
④硅-做光导纤维
⑤Na2O2-呼吸面具的供氧剂
⑥NaClO-漂白纺织物.
①ClO2-消毒剂
②NaHCO3-治疗胃酸过多
③明矾-做干燥剂
④硅-做光导纤维
⑤Na2O2-呼吸面具的供氧剂
⑥NaClO-漂白纺织物.
| A、②④⑤⑥ | B、①②⑤⑥ |
| C、①②④⑤ | D、全部 |
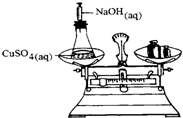 将一密闭的化学反应装置在天平上称量(如图所示).当在溶液中注入氢氧化钠溶液之后,下列叙述正确的是( )
将一密闭的化学反应装置在天平上称量(如图所示).当在溶液中注入氢氧化钠溶液之后,下列叙述正确的是( )| A、会有沉淀产生,天平左盘质量增加 |
| B、有气体产生,天平左盘质量减少 |
| C、此实验可用于说明化学反应的质量守恒 |
| D、本反应的离子方程式为:CuSO4+2OH-═Cu(OH)2↓+SO42- |
已知BaCO3和BaSO4均为难溶电解质,其溶度积分别为Ksp(BaCO3)=5.1×10-9mol2?L-2,Ksp(BaSO4)=1.1×10-10 mol2?L-2,则下列说法中正确的是( )
| A、BaSO4可做钡餐而BaCO3不能是因为Ksp(BaSO4)<Ksp(BaCO3) |
| B、在制腈纶纤维的1 L溶液中含SO42-为1.0×10-3 mol,则加入0.01 mol BaCl2不能使SO42-完全沉淀 |
| C、在清理有关仪器的BaSO4沉淀时,常加入饱和Na2CO3溶液,使BaSO4转化为BaCO3再用酸处理 |
| D、用稀H2SO4洗涤BaSO4效果比用水好,BaCO3也能用此法处理 |
已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,(MgF2的溶度积常数Ksp=7.4×10-11)取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
| A、所得溶液中的c(H+)=1.0×10-13mol?L-1 |
| B、所得溶液中由水电离产生的c(OH-)=1.0×10-13 mol?L-1 |
| C、所得溶液中的c(Mg2+)=5.6×10-10 mol?L-1 |
| D、298K时,饱和Mg(OH)2的溶液与饱和MgF2溶液相比前者的c(Mg2+)大 |
类比推断法是研究物质性质的常用方法之一,可预测许多物质的性质.但类比推断法是相对的,不能违背客观实际.下列说法正确的是( )
| A、由溶解性CaCO3<Ca(HCO3)2,则溶解性Na2CO3<NaHCO3 |
| B、向Ca(ClO)2溶液中通入少量CO2可得到CaCO3,则向Ca(ClO)2溶液中通入少量SO2可得到CaSO3 |
| C、由O2与Li加热生成Li2O,则O2与Na加热生成Na2O |
| D、有Fe与S加热生成FeS,则Cu与S加热生成Cu2S |
下列反应中硫酸既表现氧化性,又表现酸性的有( )
A、2H2SO4(浓)+Cu
| ||||
B、2H2SO4 (浓)+C
| ||||
C、H2SO4 (浓)+NaCl
| ||||
| D、H2SO4+Na2SO3═Na2SO4+H2O+SO2↑ |