题目内容
12.已知:2Na[Al(OH)4]+CO2+3H2O=2Al(OH)3↓+Na2CO3.向含2mol NaOH、1mol Ba(OH)2、2mol Na[Al(OH)4]的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量关系不正确的是( )| 选项 | A | B | C | D |
| n(CO2)(mol) | 6 | 4 | 3 | 2 |
| n(沉淀)(mol) | 2 | 3 | 2 | 1 |
| A. | A | B. | B | C. | C | D. | D |
分析 Al(OH)3能溶于强酸强碱溶液,NaOH、1mol Ba(OH)2都是强碱,且二氧化碳和NaOH反应不生成沉淀、和Ba(OH)2反应生成沉淀,所以其反应先后顺序是Ba(OH)2、NaOH、Na[Al(OH)4]、Na2CO3、BaCO3,发生的反应为:CO2+Ba(OH)2=BaCO3↓+H2O、2NaOH+CO2=Na2CO3+H2O、2Na[Al(OH)4]+CO2=2Al(OH)3↓+H2O+Na2CO3;若二氧化碳过量,还发生Na2CO3+CO2+H2O=2NaHCO3、BaCO3+CO2+H2O=Ba(HCO3)2,根据各个物理量之间的关系式计算.
解答 解:Al(OH)3能溶于强酸强碱溶液,NaOH、1mol Ba(OH)2都是强碱,且二氧化碳和NaOH反应不生成沉淀、和Ba(OH)2反应生成沉淀,所以其反应先后顺序是Ba(OH)2、NaOH、Na[Al(OH)4]、Na2CO3、BaCO3,反应方程式分别为:
CO2+Ba(OH)2=BaCO3↓+H2O、
2NaOH+CO2=Na2CO3+H2O、
2Na[Al(OH)4]+CO2=2Al(OH)3↓+H2O+Na2CO3;
若二氧化碳过量,还发生Na2CO3+CO2+H2O=2NaHCO3、
BaCO3+CO2+H2O=Ba(HCO3)2,
A.如果通入n(CO2)=6mol,1molBa(OH)2消耗1mol二氧化碳、2molNaOH消耗1mol二氧化碳、2molNa[Al(OH)4]消耗1mol二氧化碳,同时生成1mol碳酸钡、1mol碳酸钠,1mol碳酸钡、1mol碳酸钠分别消耗1mol二氧化碳,则最终二氧化碳有剩余,沉淀为氢氧化铝,为2mol,故A不选;
B.通入4mol二氧化碳,先发生反应:Ba(OH)2+CO2=BaCO3↓+H2O,消耗1mol二氧化碳,生成1mol碳酸钡沉淀,剩余3mol二氧化碳与氢氧化钠发生反应:CO2+NaOH=NaHCO3,消耗二氧化碳2mol,最后1mol二氧化碳与Na[Al(OH)4]发生反应2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3,生成2mol氢氧化铝沉淀,故生成沉淀总物质的量为3mol,故B不选;
C.当通入的n(CO2)=3 mol时,发生的离子反应是Ba2++2OH-+CO2=BaCO3↓+H2O、2OH-+CO2=CO32-+H2O、2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3,所以产生的沉淀是BaCO3和Al(OH)3且n(沉淀)之和是3mol(1mol BaCO3和2mol Al(OH)3),故C选;
D.通入2mol二氧化碳,先发生反应:Ba(OH)2+CO2=BaCO3↓+H2O,消耗1mol二氧化碳,生成1mol碳酸钡沉淀,剩余的1mol二氧化碳与2mol氢氧化钠反应恰好反应,CO2+2NaOH=Na2CO3+H2O,则沉淀只有1mol,故D不选;
故选C.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的先后顺序及反应原理为解答关键,侧重考查学生的分析、理解能力及化学计算能力,注意反应先后顺序,为易错题.

 天天向上口算本系列答案
天天向上口算本系列答案| A. | 由同种元素组成的物质肯定是纯净物 | |
| B. | 一种元素可形成多种离子 | |
| C. | 含有金属元素的离子一定都是阳离子 | |
| D. | 具有相同质子数的粒子都属于同种元素 |
| A. | 1:2 | B. | 1:5 | C. | 1:10 | D. | 10:1 |
| A. | 构成原电池正极和负极的材料必须是两种活动性不同的金属 | |
| B. | 由CH4、O2和KOH构成的燃料电池中,通入CH4的电极为正极 | |
| C. | 原电池工作时,负极发生氧化反应,化合价降低 | |
| D. | 铜锌原电池工作时,当有13 g锌溶解时,电路中有0.4 mol电子通过 |
 ,该反应的原子利用率为100%,反应的化学方程式为2CH2=CH2+O2$→_{△}^{Ag}$
,该反应的原子利用率为100%,反应的化学方程式为2CH2=CH2+O2$→_{△}^{Ag}$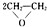 .
. ,
, ,
,