题目内容
14.烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应.如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子--丁烯和乙烯.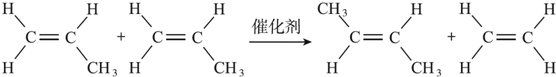
现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G.I和G在不同条件下反应可生成多种化工产品,如环酯J.
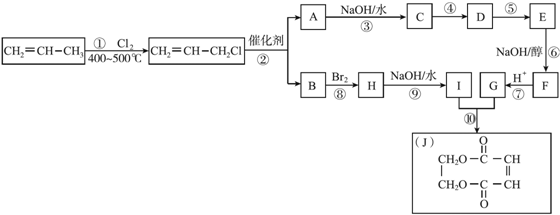
请按要求填空:
(1)写出下列反应的反应类型:①取代反应,⑥消去反应,⑧加成反应.
(2)反应②的化学方程式是2CH2=CH-CH2Cl$\stackrel{催化剂}{→}$
 +CH2=CH2.
+CH2=CH2.(3)反应④、⑤中有一反应是与HCl加成,该反应是④(填反应序号)设计这一步反应的目的是保护A分子中>C=C<不被氧化,物质E的结构简式是HOOCCH2CHClCOOH.
(4)反应⑨的化学方程式:BrCH2CH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaBr.
(5)反应⑩的化学方程式:HOCH2CH2OH+HOOC-CH=CH-COOH$?_{△}^{浓硫酸}$
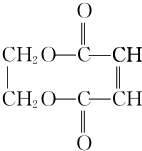 +2H2O.
+2H2O.
分析 根据J的结构简式及G的分子式为C4H4O4.可推知G为HOOC-CH=CH-COOH,I为HOCH2-CH2OH,根据各物质的转化关系及条件可反推得H为BrCH2CH2Br,B为CH2=CH2,B与溴发生加成反应生成H,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,由反应信息可知,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,故A为ClCH2CH=CHCH2Cl,根据A在氢氧化钠水溶液、加热条件下发生取代反应生成C,C为HOCH2CH=CHCH2OH,E发生消去反应生成F,F酸化得到G,故F为NaOOC-CH=CH-COONa,E为HOOCCH2CHClCOOH,结合E和DC的结构可知,D为HOCH2CH2CHClCH2OH,C与HCl发生加成反应反应生成D,保护C=C不被氧化,D再氧化可得E,据此分析解答.
解答 解:根据J的结构简式及G的分子式为C4H4O4.可推知G为HOOC-CH=CH-COOH,I为HOCH2-CH2OH,根据各物质的转化关系及条件可反推得H为BrCH2CH2Br,B为CH2=CH2,B与溴发生加成反应生成H,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,由反应信息可知,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,故A为ClCH2CH=CHCH2Cl,根据A在氢氧化钠水溶液、加热条件下发生取代反应生成C,C为HOCH2CH=CHCH2OH,E发生消去反应生成F,F酸化得到G,故F为NaOOC-CH=CH-COONa,E为HOOCCH2CHClCOOH,结合E和DC的结构可知,D为HOCH2CH2CHClCH2OH,C与HCl发生加成反应反应生成D,保护C=C不被氧化,D再氧化可得E,
(1)通过以上分析知,①⑥⑧的反应类型分别是取代反应、消去反应、加成反应,
故答案为:取代反应;消去反应;加成反应;
(2)该反应方程式为2CH2=CH-CH2Cl$\stackrel{催化剂}{→}$  +CH2=CH2,故答案为:2CH2=CH-CH2Cl$\stackrel{催化剂}{→}$
+CH2=CH2,故答案为:2CH2=CH-CH2Cl$\stackrel{催化剂}{→}$  +CH2=CH2;
+CH2=CH2;
(3)反应④、⑤中有一反应是与HCl加成,该反应是④,设计这一步反应的目的是 保护A分子中>C=C<不被氧化,物质E的结构简式是HOOCCH2CHClCOOH,
故答案为:④;保护A分子中>C=C<不被氧化;HOOCCH2CHClCOOH;
(4)该反应方程式为BrCH2CH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaBr,故答案为:BrCH2CH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaBr;
(5)该反应方程式为HOCH2CH2OH+HOOC-CH=CH-COOH$?_{△}^{浓硫酸}$ +2H2O,
+2H2O,
故答案为:HOCH2CH2OH+HOOC-CH=CH-COOH$?_{△}^{浓硫酸}$ +2H2O.
+2H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识综合应用能力,根据官能团及其性质关系结合题给信息分析解答,知道常见有机物反应类型及反应条件,题目难度中等.

| A. | 1.0Ll.0mol.L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA | |
| C. | 25C时pH=11的Na2C03溶液中水电离出的OH-的数目为0.001NA | |
| D. | 氧原子总数为0.2NA的S02和O2的混合气体,其体积为2.24L |
| A. | 刚玉--SiO2 | B. | 明矾--Al2(SO4)3•12H2O | ||
| C. | 小苏打--Na2CO3 | D. | 漂白粉--Ca(ClO)2、CaCl2 |
| 实验操作 | 实验现象 | 结论 |
| 在一杯浑浊的水中加 少量Al2(SO4)3静置 | 烧杯中的水变澄清 | Al2(SO4)3可 以净水 |
| 在一杯浑浊的水中加 少量KCl,静置 | 烧杯中的水 仍然浑浊 | K+不能起净水作用 |
| A. | 除去锅炉的水垢:CaCO3+SO42-?CaSO4+CO32- | |
| B. | 电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 实验室制氯气:KClO3+6H37Cl(浓)═KCl+337Cl2↑+3H2O | |
| D. | HCO3-的水解:HCO3-+H2O?CO32-+H3O+ |
| A. | 少量过氧化钠投入AlCl3溶液 | B. | FeCl3溶液与NaHCO3溶液混合加热 | ||
| C. | Ba(OH)2溶液与(NH4)2SO4 | D. | 明矾溶液与小苏打溶液混合 |
 ,下列可以验证C与D两元素原子得电子能力强弱的事实是BCD(填编号).
,下列可以验证C与D两元素原子得电子能力强弱的事实是BCD(填编号).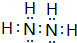 ;C的另一种氢化物与D的一种氢化物的电子总数相等,实验室制取C的该气态氢化物的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
;C的另一种氢化物与D的一种氢化物的电子总数相等,实验室制取C的该气态氢化物的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.