题目内容
2.已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )| A. | 升高温度,溶液的pH和电离平衡常数均减小 | |
| B. | 该溶液的pH=4 | |
| C. | 此酸的电离平衡常数约为1×10-7 | |
| D. | 加入少量纯HA,电离程度和电离平衡常数均减小 |
分析 A.HA电离吸热,升高温度,促进电离;
B.c(H+)=0.1mol/L×0.1%=1×10-4,pH=-lgc(H+);
C.Ka=$\frac{c({H}^{+})c({A}^{-})}{c(HA)}$;
D.加入少量纯HA,浓度增大,电离程度减小,但Ka与温度有关、与浓度无关.
解答 解:A.HA电离吸热,升高温度,促进电离,则氢离子浓度增大,溶液的pH减小,而电离平衡常数增大,故A错误;
B.c(H+)=0.1mol/L×0.1%=1×10-4,pH=-lgc(H+)=4,故B正确;
C.此酸的电离平衡常数Ka=$\frac{c({H}^{+})c({A}^{-})}{c(HA)}$=$\frac{1{0}^{-4}×1{0}^{-4}}{0.1}$=1×10-7,故C正确;
D.加入少量纯HA,浓度增大,电离程度减小,但Ka与温度有关、与浓度无关,则电离平衡常数不变,故D错误;
故选AD.
点评 本题考查弱电解质的电离,为高频考点,把握电离常数的影响因素及计算为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点,题目难度不大.

练习册系列答案
相关题目
12.下列有关化学用语表示正确的是( )
| A. | CaH2的电子式为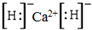 | |
| B. | Cl-的结构示意图: | |
| C. | 质子数为92、中子数为146的U原子:${\;}_{92}^{146}$U | |
| D. | 2,4,6-三硝基苯甲酸结构简式: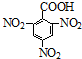 |
13.下列实验操作顺序或方法正确的是( )
| A. | 把苯和浓溴水混合后加入FeBr3可制溴苯 | |
| B. | 浓硫酸与浓硝酸混合冷却后,边滴入苯边振荡,在60℃水浴中加热可制硝基苯 | |
| C. | 乙烷中混有乙烯,通入氢气与乙烯反应可达到除杂的目的 | |
| D. | 乙烯通入水中可制得酒精 |
10.下列化学用语正确的是( )
| A. | 聚丙烯的结构简式:CH2-CH2-CH2 | B. | 丙烷分子的比例模型: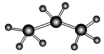 | ||
| C. | 四氯化碳分子的电子式: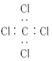 | D. | 1丁烯分子的键线式: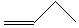 |
17.将下列固体物质溶于水,再将其溶液加热、蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是( )
| A. | FeCl3 | B. | NaAlO2 | C. | NaHCO3 | D. | Na2SO3 |
7.某学生对Na2SO3与AgNO3在不同 pH 下的反应进行探究.
(1)测得Na2SO3溶液 pH=10、AgNO3 溶液 pH=5.
(2)调节 pH,实验记录如表:
查阅资料得知:
ⅰ.Ag2SO3:白色,难溶于水,溶于过量的Na2SO3 溶液.
ⅱ.Ag2O:棕黑色,不溶于水,能和酸反应.
该学生对 a 中的白色沉淀提出了两种假设:
①白色沉淀为Ag2SO3
②白色沉淀为Ag2SO4,推测的依据是SO32-有还原性,可能被氧化为SO42-,与Ag+反应生成Ag2SO4白色沉淀.
(3)取 b、c 中白色沉淀,置于Na2SO3溶液中,沉淀溶解.该同学设计实验确认了白色沉淀不是Ag2SO4.实验方法是:另取Ag2SO4固体置于Na2SO3溶液中,未溶解.
(4)将 c 中 X 滤出、洗净,为确认其组成,实验如下:
Ⅰ.向 X 中滴加稀盐酸,无明显变化.
Ⅱ.向 X 中加入过量浓硝酸,产生红棕色气体.
Ⅲ.用Ba(NO3)2、BaCl2溶液检验Ⅱ中反应后的溶液,前者无明显变化,后者产生白色
沉淀.
①实验Ⅰ的目的是检验棕黑色物质X是否为Ag2O.
②根据上述现象,分析 X 的成分是Ag.
③Ⅱ中反应的化学方程式是Ag+2HNO3(浓)═AgNO3+NO2↑+H2O.
(5)该同学综合以上实验,分析 X 产生的原因是:随着酸性的增强,体系的还原性强.
(1)测得Na2SO3溶液 pH=10、AgNO3 溶液 pH=5.
(2)调节 pH,实验记录如表:
| 实验 | pH | 现象 |
| a | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
| b | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
| c | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质X |
ⅰ.Ag2SO3:白色,难溶于水,溶于过量的Na2SO3 溶液.
ⅱ.Ag2O:棕黑色,不溶于水,能和酸反应.
该学生对 a 中的白色沉淀提出了两种假设:
①白色沉淀为Ag2SO3
②白色沉淀为Ag2SO4,推测的依据是SO32-有还原性,可能被氧化为SO42-,与Ag+反应生成Ag2SO4白色沉淀.
(3)取 b、c 中白色沉淀,置于Na2SO3溶液中,沉淀溶解.该同学设计实验确认了白色沉淀不是Ag2SO4.实验方法是:另取Ag2SO4固体置于Na2SO3溶液中,未溶解.
(4)将 c 中 X 滤出、洗净,为确认其组成,实验如下:
Ⅰ.向 X 中滴加稀盐酸,无明显变化.
Ⅱ.向 X 中加入过量浓硝酸,产生红棕色气体.
Ⅲ.用Ba(NO3)2、BaCl2溶液检验Ⅱ中反应后的溶液,前者无明显变化,后者产生白色
沉淀.
①实验Ⅰ的目的是检验棕黑色物质X是否为Ag2O.
②根据上述现象,分析 X 的成分是Ag.
③Ⅱ中反应的化学方程式是Ag+2HNO3(浓)═AgNO3+NO2↑+H2O.
(5)该同学综合以上实验,分析 X 产生的原因是:随着酸性的增强,体系的还原性强.
14.下列对化学反应的认识错误的是( )
| A. | 一定会有新物质生成 | B. | 一定伴随着能量的变化 | ||
| C. | 可能会引起物质状态的变化 | D. | 有化学键破坏的一定是化学反应 |
12.下列分离或提纯物质的方法正确的是( )
| A. | 用过滤的方法分离氢氧化铁胶体和氯化铁溶液 | |
| B. | 用汽油萃取溴水中的溴 | |
| C. | 用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钾 | |
| D. | 用分液可分离乙酸乙酯和乙醇混合物 |