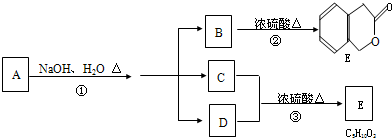
题目内容
现有三种物质A、B、C,其中有一种是酸,一种是碱,一种是盐,溶于水后电离,可以产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果填空:
(1)物质A溶于水的电离方程式为 .
(2)写出下列反应的离子方程式:A溶液与C溶液反应: ;B与C反应至溶液呈中性: .
(3)鉴别B溶液中阴离子的实验方法是 .
(4)D与E的混合物a g,加入足量盐酸,反应完全生成标准状况时的气体b L,则D在混合物中的质量分数为 .
| 阳离子 | Na+ H+ Ba2+ | ||||
| 阴离子 | OH- CO
|
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果填空:
(1)物质A溶于水的电离方程式为
(2)写出下列反应的离子方程式:A溶液与C溶液反应:
(3)鉴别B溶液中阴离子的实验方法是
(4)D与E的混合物a g,加入足量盐酸,反应完全生成标准状况时的气体b L,则D在混合物中的质量分数为
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题,计算题
分析:生成的气体只有CO2符合,发生的反应为 2H++CO32-=H2O+CO2↑,CO2气体可以和C溶液反应生成沉淀E,则C为Ba(OH)2,沉淀E为BaCO3,E与B溶液反应,则B为H2SO4,所以A为Na2CO3,B、C反应生成的沉淀D为BaSO4,根据物质的性质和反应的有关方程式解答该题.
解答:
解:生成的气体只有CO2符合,发生的反应为 2H++CO32-=H2O+CO2↑,CO2气体可以和C溶液反应生成沉淀E,则C为Ba(OH)2,沉淀E为BaCO3,E与B溶液反应,则B为H2SO4,所以A为Na2CO3,B、C反应生成的沉淀D为BaSO4.
(1)A为Na2CO3,属于强电解质,在水中完全电离,电离方程式为:Na2CO3═2Na++CO32-;
故答案为:Na2CO3═2Na++CO32-;
(2)A为Na2CO3,C为Ba(OH)2,二者发生复分解反应生成碳酸钡沉淀和氢氧化钠,离子方程式为:
Ba2++CO32-═BaCO3↓;则B为H2SO4,C为Ba(OH)2,二者反应生成硫酸钡和水,反应的离子方程式为:
2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O;
故答案为:Ba2++CO32-═BaCO3↓;2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O;
(3)检验SO42-时,取溶液少量,先加盐酸,无明显现象,再加BaCl2溶液产生白色沉淀,证明有SO42-;
故答案为:取溶液少量,先加盐酸,无明显现象,再加BaCl2溶液产生白色沉淀;
(4)D与E的混合物ag,加入足量盐酸,发生的反应为BaCO3+2HCl=CO2↑+BaCl2+H2O,
n(CO2)=
mol,
n(BaCO3)=n(CO2)=
mol,
m(BaCO3)=
mol×197g/mol=
g,
m(BaSO4)=ag-
g,
所以:w(BaSO4)=
×100%=
×100%;
故答案为:
×100%.
(1)A为Na2CO3,属于强电解质,在水中完全电离,电离方程式为:Na2CO3═2Na++CO32-;
故答案为:Na2CO3═2Na++CO32-;
(2)A为Na2CO3,C为Ba(OH)2,二者发生复分解反应生成碳酸钡沉淀和氢氧化钠,离子方程式为:
Ba2++CO32-═BaCO3↓;则B为H2SO4,C为Ba(OH)2,二者反应生成硫酸钡和水,反应的离子方程式为:
2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O;
故答案为:Ba2++CO32-═BaCO3↓;2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O;
(3)检验SO42-时,取溶液少量,先加盐酸,无明显现象,再加BaCl2溶液产生白色沉淀,证明有SO42-;
故答案为:取溶液少量,先加盐酸,无明显现象,再加BaCl2溶液产生白色沉淀;
(4)D与E的混合物ag,加入足量盐酸,发生的反应为BaCO3+2HCl=CO2↑+BaCl2+H2O,
n(CO2)=
| b |
| 22.4 |
n(BaCO3)=n(CO2)=
| b |
| 22.4 |
m(BaCO3)=
| b |
| 22.4 |
| 197b |
| 22.4 |
m(BaSO4)=ag-
| 197b |
| 22.4 |
所以:w(BaSO4)=
ag-
| ||
| ag |
| 22.4a-197b |
| 22.4a |
故答案为:
| 22.4a-197b |
| 22.4a |
点评:本题考查较为综合,涉及离子的推断、离子方程式的书写,离子的检验及混合物的计算,题目难度中等,注意根据物质的性质判断物质的成分为解答该题的关键.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
水的电离过程为H2O?H++OH-,在25℃时水的离子积为KW=1.0×10-14,在35℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )
| A、c(H+)随着温度的升高而降低 |
| B、35℃时c(H+)>c(OH-) |
| C、35℃时的水比25℃时的水电离程度小 |
| D、水的电离是个吸热过程 |
下列表示对应化学反应的离子方程式正确的是( )
| A、硫酸铝溶液中滴加过量浓氨水:Al3++4OH-═AlO2-+2H2O |
| B、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
| C、碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O |
| D、过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
某无色溶液中只可能溶有NH4+、K+、Al3+、Mg2+、HCO3-、Cl-、I-、MnO4-、SO42-等离子中的几种离子.分析其组成,现进行如下实验:
①取l0mL该溶液于试管中滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲.
②取上述反应后的滤液,加入AgNO3溶液未见沉淀产生.
③另取l0mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加人NaOH的物质的量为0.03mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为0.224L(假设丙全部逸出),最后沉淀完全溶解.下列推断正确的是( )
①取l0mL该溶液于试管中滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲.
②取上述反应后的滤液,加入AgNO3溶液未见沉淀产生.
③另取l0mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加人NaOH的物质的量为0.03mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为0.224L(假设丙全部逸出),最后沉淀完全溶解.下列推断正确的是( )
| A、肯定有K+、Al3+、Mg2+、SO42- |
| B、肯定有K+、NH4+、Al3+、SO42- |
| C、肯定没有K+、HCO3-、MnO4- |
| D、肯定没有K+、NH4+、Cl- |
某溶液中可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+,进行如下实验:
(1)取该溶液100mL,加入过量NaOH溶液,加热,得到0.01 mol 气体,同时产生红褐色沉淀;过滤,将沉淀洗涤,灼烧,得到0.8 g固体;
(2)向(1)的滤液中通入足量CO2,过滤,得到0.01 mol沉淀;
(3)向(2)的滤液中加入足量用盐酸酸化的BaCl2溶液,得到2.33g沉淀,
由此可知原溶液中( )
(1)取该溶液100mL,加入过量NaOH溶液,加热,得到0.01 mol 气体,同时产生红褐色沉淀;过滤,将沉淀洗涤,灼烧,得到0.8 g固体;
(2)向(1)的滤液中通入足量CO2,过滤,得到0.01 mol沉淀;
(3)向(2)的滤液中加入足量用盐酸酸化的BaCl2溶液,得到2.33g沉淀,
由此可知原溶液中( )
| A、至少存在CO32-、Cl-中的一种 |
| B、Cl-一定存在,K+可能存在 |
| C、Cl-一定存在,且c(Cl-)≥0.6mol?L-1 |
| D、溶液中至少存在4种离子 |
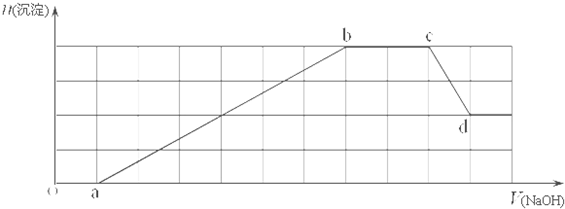
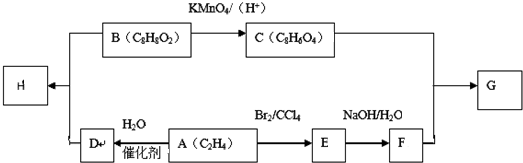
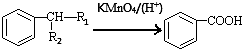 (-R1、-R2表示氢原子或烃基)
(-R1、-R2表示氢原子或烃基)