题目内容
某工厂排放的酸性废水中含有较多的Cu2+,对农作物和人畜都有害,欲采用化学法除去有害成分,最好是加入下列物质中的( )
| A、食盐、硫酸 |
| B、胆矾、石灰水 |
| C、铁粉、生石 |
| D、苏打、盐 |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:
分析:酸性废水中含有较多的Cu2+,除去铜离子选择比铜活泼的金属与碱,降低溶液的酸性可选择碱,以此来解答.
解答:
解:A.NaCl不参加反应,加硫酸使酸性增强,故A错误;
B.因胆矾中含有Cu2+,这样不但没有除去酸性废水中含有较多的Cu2+,反而更多,再加入石灰水消耗化学试剂增多,故B错误;
C.因Fe粉可以置换出Cu,加入的生石灰,一则可以中和酸性,二则CaO与H2O反应生成的Ca(OH)2可以使Cu2+、Fe2+等变成沉淀析出,故C正确;
D.苏打与酸反应,但加入的盐不明确,盐中可能含重金属离子如氯化钡,故D错误;
故选C.
B.因胆矾中含有Cu2+,这样不但没有除去酸性废水中含有较多的Cu2+,反而更多,再加入石灰水消耗化学试剂增多,故B错误;
C.因Fe粉可以置换出Cu,加入的生石灰,一则可以中和酸性,二则CaO与H2O反应生成的Ca(OH)2可以使Cu2+、Fe2+等变成沉淀析出,故C正确;
D.苏打与酸反应,但加入的盐不明确,盐中可能含重金属离子如氯化钡,故D错误;
故选C.
点评:本题考查物质分离、提纯的方法及选择,为高频考点,把握物质的性质及分离方法为解答的关键,侧重除杂的考查,注意物质的性质及发生的化学反应,题目难度不大.

练习册系列答案
相关题目
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、状态A时I2的转化率比状态B的小 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C、若反应进行到状态D时,一定有v正>v逆 |
| D、状态A与状态B相比,状态A的c(I2)大 |
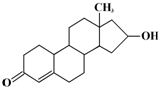 “诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图.下列关于“诺龙”的说法中不正确的是( )
“诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图.下列关于“诺龙”的说法中不正确的是( )| A、分子式是C18H26O2 |
| B、具有酚的化学性质 |
| C、具有烯的化学性质 |
| D、具有酮的化学性质 |
钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2═2Fe(OH)2.以下说法正确的是( )
| A、负极发生的反应为:Fe-2e-=Fe2+ |
| B、正极发生的反应为:4OH--4e-═2H2O+O2↑ |
| C、原电池是将电能转变为化学能的装置 |
| D、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
 B.
B. C.
C.