题目内容
14.单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备,其中X为Z的氧化物,Y为氢化物,分子结构与甲烷相似,回答下列问题: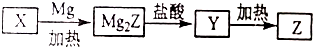
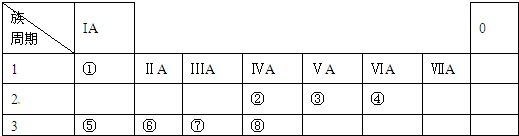
(1)Z在元素周期表中的位置第三周期IVA族,X中化学键的类型是共价键.
(2)由Mg2Z生成Y的化学反应方程式为Mg2Si+4HCl=2 MgCl2+SiH4↑,Y分子的电子式为
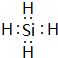 .
.(3)能与X发生化学反应的酸是氢氟酸;由X制备Mg2Z的化学方程式为SiO2+4Mg$\frac{\underline{\;加热\;}}{\;}$2MgO+Mg2Si.
分析 单质Z是一种常见的半导体材料,则Z为Si,X为Z的氧化物,则X为SiO2,Y为氢化物,分子结构与甲烷相似,则Y为SiH4,加热SiH4分解得到Si与氢气,据此解答.
解答 解:单质Z是一种常见的半导体材料,则Z为Si,X为Z的氧化物,则X为SiO2,Y为氢化物,分子结构与甲烷相似,则Y为SiH4,加热SiH4分解得到Si与氢气.
(1)Z为Si,在元素周期表中的位置:第三周期IVA族,X为SiO2,含有的化学键属于共价键,
故答案为:第三周期IVA族;共价键;
(2)由Mg2Z生成Y的化学反应方程式为:Mg2Si+4HCl=2 MgCl2+SiH4↑,Y为SiH4,电子式为 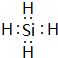 ,
,
故答案为:Mg2Si+4HCl=2 MgCl2+SiH4↑;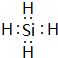 ;
;
(3)能与SiO2发生化学反应的酸是氢氟酸,由SiO2制备Mg2Si的化学方程式为:SiO2+4Mg$\frac{\underline{\;加热\;}}{\;}$2MgO+Mg2Si,
故答案为:氢氟酸;SiO2+4Mg$\frac{\underline{\;加热\;}}{\;}$2MgO+Mg2Si.
点评 本题考查无机物推断,关键是确定Z为硅,再结合转化关系分析,是对学生综合能力的考查,难度中等.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
5.已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=akJ•mol-1,平衡常数为K测得在不同温度下,K值如下:
(1)写成该反应的平衡常数表达式$\frac{[CO]}{[C{O}_{2}]}$.
(2)该反应为吸热(选填“吸热”或“放热”)反应.
(3)700℃时反应达到平衡状态,要使该平衡向右移动,其他条件不变时,可以采取的措施有BC(填序号).
A.缩小反应器体积 B.通入CO2C.升高温度到900℃D.使用合适的催化剂 E.增加Fe的量
(4)下列图象符合该反应的是A(填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2).

| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(2)该反应为吸热(选填“吸热”或“放热”)反应.
(3)700℃时反应达到平衡状态,要使该平衡向右移动,其他条件不变时,可以采取的措施有BC(填序号).
A.缩小反应器体积 B.通入CO2C.升高温度到900℃D.使用合适的催化剂 E.增加Fe的量
(4)下列图象符合该反应的是A(填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2).

9.某体系中的物质有HCl、NaCl、FeCl2、H2O、NaNO3、FeCl3、NO,FeCl2为反应物,则下列有关说法正确的是( )
| A. | NO在反应中作还原剂 | |
| B. | 氧化剂和还原剂的物质的量比为1:3 | |
| C. | FeCl2发生还原反应 | |
| D. | 0.5molFeCl2发生反应,转移电子1.5mol |
19.下列有关仪器使用方法或实验操作正确的是( )
| A. | 洗净的滴定管和容量瓶可以放进烘箱中烘干 | |
| B. | 用10mL量筒量取10.00mLNaCl溶液 | |
| C. | 酸式滴定管装标准溶液前,必须先用该溶液润洗2~3次 | |
| D. | 用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体 |
6.下列说法正确的是( )
| A. | 碱金属的单质中,锂的还原性最强 | |
| B. | 第ⅠA族元素比第ⅡA族元素的金属性强 | |
| C. | 随着核电荷数的递增,卤族元素的气态氢化物的稳定性逐渐减弱 | |
| D. | 随着核电荷数的递增,第三周期元素的氧化物对应的水化物的酸性逐渐增强. |
3.氨基甲酸铵(NH2COONH4)是一种白色固体,受热易分解.某小组模拟制备氨基甲酸铵,反应如下(且温度对反应的影响比较灵敏):2NH3(g)+CO2(g)?NH2COONH4(s)△H<0
(1)如用下图I装置制取氨气,可选择的试剂是浓氨水与氢氧化钠固体(或浓氨水与碱石灰或浓氨水与生石灰).
(2)制备氨基甲酸铵的装置如图Ⅱ所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中. 当悬浮物较多时,停止制备.
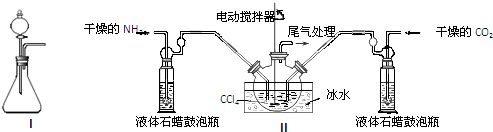
注:CCl4与液体石蜡均为惰性介质.
①发生器用冰水冷却的原因是降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解).液体石蜡鼓泡瓶的作用是通过观察气泡,调节NH3与CO2通入比例(或通过观察气泡,控制NH3与CO2的反应速率).
②从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是C(填写选项序号).
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种.
①设计方案,进行成分探究.
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸.
②根据①的结论:取氨基甲酸铵样品6.58g,用足量氢氧化钡溶液充分处理后,过滤、洗涤、干燥,测得沉淀质量为3.94g.则样品中氨基甲酸铵的质量分数为76%..
[保留两位有效数字,已知Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(BaCO3)=197].
(1)如用下图I装置制取氨气,可选择的试剂是浓氨水与氢氧化钠固体(或浓氨水与碱石灰或浓氨水与生石灰).
(2)制备氨基甲酸铵的装置如图Ⅱ所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中. 当悬浮物较多时,停止制备.

注:CCl4与液体石蜡均为惰性介质.
①发生器用冰水冷却的原因是降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解).液体石蜡鼓泡瓶的作用是通过观察气泡,调节NH3与CO2通入比例(或通过观察气泡,控制NH3与CO2的反应速率).
②从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是C(填写选项序号).
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种.
①设计方案,进行成分探究.
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解. | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置 | 溶液不变浑浊,证明固体中不含碳酸铵. |
| 步骤3:向试管中继续加入少量澄清石灰水. | 溶液变浑浊,证明固体中含有碳酸氢铵. |
[保留两位有效数字,已知Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(BaCO3)=197].
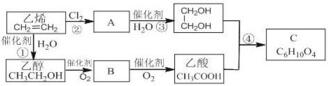
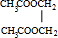 +2H2O.
+2H2O. )与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点.完成下列填空:
)与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点.完成下列填空: 或
或 .
. .
. 与氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色.A的结构简式为
与氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色.A的结构简式为 .由A生成对溴苯乙烯的反应条件为浓硫酸、加热.
.由A生成对溴苯乙烯的反应条件为浓硫酸、加热.