题目内容
溴是海水中重要的非金属元素,下列有关说法中正确的是( )
| A、从海水中提取溴时,不涉及氧化还原反应 |
| B、液溴的保存用带橡胶塞的棕色试剂瓶 |
| C、可以用CCl4萃取溴水中的溴 |
| D、向FeBr2溶液中通入Cl2时,一定会发生如下反应:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:A、海水中溴以离子形式存在,需要氧化还原反应生成溴单质;
B、液溴能腐蚀橡胶,不能保存在带橡胶塞的棕色试剂瓶;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶;
D、Fe2+的还原性强于溴离子点的还原性,若氯气少量,只氧化Fe2+.
B、液溴能腐蚀橡胶,不能保存在带橡胶塞的棕色试剂瓶;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶;
D、Fe2+的还原性强于溴离子点的还原性,若氯气少量,只氧化Fe2+.
解答:
解:A、海水中溴以离子形式存在,需要氧化还原反应生成溴单质,故A错误;
B、液溴能腐蚀橡胶,不能保存在带橡胶塞的棕色试剂瓶,可以用水密封避光保存,故B错误;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶,可以用CCl4萃取溴水中的溴,故C正确;
D、Fe2+的还原性强于溴离子点的还原性,若氯气少量,只氧化Fe2+,若氯气过量,一定会全部氧化Fe2+和溴离子,故D错误.
故选:C.
B、液溴能腐蚀橡胶,不能保存在带橡胶塞的棕色试剂瓶,可以用水密封避光保存,故B错误;
C、溴在CCl4中溶解度大于在水中的溶解度,且CCl4和水不混溶,可以用CCl4萃取溴水中的溴,故C正确;
D、Fe2+的还原性强于溴离子点的还原性,若氯气少量,只氧化Fe2+,若氯气过量,一定会全部氧化Fe2+和溴离子,故D错误.
故选:C.
点评:本题考查了非金属元素的性质及单质的性质与保存、应用,氧化还原反应的判断,注意氧化性Cl2>Br2>Fe3+.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
常温下,99mL0.1mol/L的盐酸和101mL0.05mol/L氢氧化钡溶液混合后,溶液的c(H+)为( )
(不考虑混合时的体积变化)
(不考虑混合时的体积变化)
| A、0.5×(10-8+10-10)mol/L |
| B、(10-8+10-10)mol/L |
| C、(1×10-14-5×10-5)mol/L |
| D、1×10-11 mol/L |
对三种金属单质a、b、c进行下表所示实验(其他条件等同);
由上表实验结果分析可知,这三种金属的还原性由强到弱的顺序是( )
| 实验 金属 | a | b | c |
| 与冷水反应 | 不反应 | 缓慢反应 | 未实验 |
| 与2mol?1-1的HCl溶液反应 | 溶解并放出气体 | 未实验 | 不反应 |
| A、a>b>c |
| B、b>a>c |
| C、a>c>b |
| D、c>b>a |
下列属于强电解质的是( )
| A、醋酸 | B、酒精 | C、铜 | D、小苏打 |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、碱性氧化物 七氧化二锰 Mn2O7 |
| B、酸性氧化物 干冰 CO |
| C、酸 硫酸 H2S |
| D、盐 纯碱 Na2CO3 |




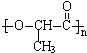 ,则形成该高聚物的单体结构简式为
,则形成该高聚物的单体结构简式为