题目内容
下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向无水乙醇中加入浓H2SO4,加热至170°C产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
| D | 向银氨溶液中加入葡萄糖溶液,水浴加热,有光亮的银镜产生 | 葡萄糖分子结构中有醛基 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.酸性条件下,亚铁离子被硝酸根离子氧化生成铁离子,同时生成NO,NO易被氧化生成二氧化氮;
B.醛基和新制氢氧化铜悬浊液的反应必须在碱性条件下,否则实验失败;
C.乙醇也能使酸性高锰酸钾溶液褪色;
D.碱性条件下,醛基和银氨溶液发生银镜反应.
B.醛基和新制氢氧化铜悬浊液的反应必须在碱性条件下,否则实验失败;
C.乙醇也能使酸性高锰酸钾溶液褪色;
D.碱性条件下,醛基和银氨溶液发生银镜反应.
解答:
解:A.向装有Fe(NO3)2溶液的试管中加入稀H2SO4,相当于溶液中含有硝酸,硝酸和亚铁离子反应生成铁离子和NO,NO不稳定为空气氧化生成二氧化氮,而不是硝酸分解生成二氧化氮,故A错误;
B.在加入新制氢氧化铜悬浊液之前应该加入NaOH溶液中和酸,否则实验不成功,故B错误;
C.乙醇具有挥发性,升高温度促进乙醇挥发,所以制取的乙烯中含有乙醇,乙醇能被酸性高锰酸钾溶液氧化而导致酸性高锰酸钾溶液褪色,所以使酸性高锰酸钾溶液褪色的气体有乙烯和乙醇,要检验乙烯的性质,应该先除去乙烯中的乙醇,故C错误;
D.醛基和银氨溶液发生银镜反应,所以向银氨溶液中加入葡萄糖溶液,水浴加热,有光亮的银镜产生,说明葡萄糖中含有醛基,故D正确;
故选D.
B.在加入新制氢氧化铜悬浊液之前应该加入NaOH溶液中和酸,否则实验不成功,故B错误;
C.乙醇具有挥发性,升高温度促进乙醇挥发,所以制取的乙烯中含有乙醇,乙醇能被酸性高锰酸钾溶液氧化而导致酸性高锰酸钾溶液褪色,所以使酸性高锰酸钾溶液褪色的气体有乙烯和乙醇,要检验乙烯的性质,应该先除去乙烯中的乙醇,故C错误;
D.醛基和银氨溶液发生银镜反应,所以向银氨溶液中加入葡萄糖溶液,水浴加热,有光亮的银镜产生,说明葡萄糖中含有醛基,故D正确;
故选D.
点评:本题考查实验方案评价,涉及物质或官能团的检验,明确物质的性质是解本题关键,该题侧重于学生的分析能力、实验能力和评价能力的考查,注意把握实验原理和操作方法,注意A中隐含条件,为易错点.

练习册系列答案
相关题目
相同碳原子数的烷烃、烯烃、炔烃,在空气中完全燃烧生成二氧化碳和水,需要空气量的比较中正确是( )
| A、烷烃最多 | B、烯烃最多 |
| C、炔烃最多 | D、三者一样多 |
你认为下列实验数据不合理的是( )
| A、用pH试纸测得某河水的pH值为6.24 |
| B、用托盘天平称得氧化铜粉末的质量为11.5g |
| C、用10ml量筒取8.5ml的溶液 |
| D、测得某粗盐中氯化钠的质量分数为90.5% |
下列有关实验的说法正确的是( )
A、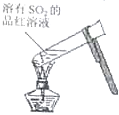 加热后溶液的颜色变为无色 |
B、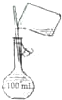 配置100mL0.01moL/L 溶液 |
C、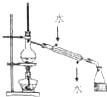 实验室用该装置制取蒸馏水 |
D、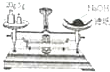 称量25克 |
在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积减半,当达到新的平衡时,A的浓度增大为原来的1.8倍,则下列说法错误的是( )
| A、平衡向正反应方向移动了 |
| B、物质A的转化率增大了 |
| C、恒温恒压时再充入A物质,达到新的平衡时A的质量分数增加了 |
| D、a>b |
有关少量食用油在低温下出现冻结现象后能否食用及解释合理的是( )
| A、不能,因为已经变质 |
| B、不能,因为含有杂质 |
| C、不能,因为含有水份 |
| D、能,因为那只是油脂主要成份在低温下结晶析出,是正常物理形态变化,并未变质 |
下列电离方程式错误的是( )
| A、CaCl2=Ca2++2Cl- |
| B、K2SO4=2 K++SO42- |
| C、HNO3=H++NO3- |
| D、NaClO=Na++Cl-+O2- |
下列叙述正确的是( )
| A、室温下,pH相同、体积相同的醋酸和盐酸两种溶液分别加水稀释2倍后,两溶液的酸性都减弱,其中,稀释后的盐酸的酸性还是比醋酸的强 |
| B、室温下,pH相同、体积相同的氨水和氢氧化钠两种溶液分别加水稀释2倍后,两溶液的pH均减小,其中,稀释后的氢氧化钠的pH比氨水的小 |
| C、室温时,0.01 mol?L-1醋酸溶液的pH=2 |
| D、室温,0.01 mol?L-1醋酸溶液中加入等体积0.01 mol?L-1 NaOH溶液后,所得溶液的pH=7 |
