题目内容
7.下列物质中的杂质(括号中是杂质)分别可以用下列什么方法除去,把字母填到相应的空格上.A、溶解过滤 B、分液 C、萃取与分液 D、洗气 E、蒸馏 F、加新制CaO再蒸馏 G、结晶或重结晶
(1)酒精(水)F
(2)壬烷(己烷)E
(3)KNO3(NaCl)G
(4)溴苯(水)B
(5)甲烷(乙烯)D
(6)NaCl(泥沙)A
(7)溴水(水)C
(8)CO2(HCl)D.
分析 (1)酒精与水互溶,但沸点不同;
(2)壬烷与己烷互溶,但沸点不同;
(3)KNO3、NaCl的溶解度受温度影响不同;
(4)溴苯与水分层;
(5)甲烷与溴水不反应,乙烯与溴水反应;
(6)泥沙不溶于水;
(7)溴不易溶于水,易溶于四氯化碳;
(8)HCl与饱和碳酸氢钠溶液反应生成二氧化碳.
解答 解:(1)酒精与水互溶,但沸点不同,则选择蒸馏法分离,故答案为:F;
(2)壬烷与己烷互溶,但沸点不同,则选择蒸馏法分离,故答案为:E;
(3)KNO3、NaCl的溶解度受温度影响不同,则选择结晶法分离,故答案为:G;
(4)溴苯与水分层,可用分液的方法分离,故答案为:B;
(5)甲烷与溴水不反应,乙烯与溴水反应,则利用洗气分离,故答案为:D;
(6)泥沙不溶于水则选择过滤分离,故答案为:A;
(7)溴不易溶于水,易溶于四氯化碳,则选择萃取、分液分离,故答案为:C;
(8)HCl与饱和碳酸氢钠溶液反应生成二氧化碳,则利用洗气分离,故答案为:D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离提纯为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.氧氟沙星是常用抗菌药,其结构简式如图所示,下列对氧氟沙星叙述错误的是( )
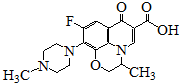

| A. | 能发生加成、取代反应 | |
| B. | 一定条件下,1mol该物质最多消耗5mol H2 | |
| C. | 分子内共有19个氢原子 | |
| D. | 分子内共平面的碳原子多于6个 |
19.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,下列说法正确的是( )
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 此有机物一定是烃CH4 | D. | 分子中可能含有氧原子 |
16.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 50g质量分数为17%的H2O2水溶液中含氧原子数目为0.5NA | |
| B. |  12g石墨烯(如图)中含有C-C键的数目为1.5NA 12g石墨烯(如图)中含有C-C键的数目为1.5NA | |
| C. | 常温下,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| D. | 一定量的Na2O2与H2O反应产生1.12L O2,则反应中转移的电子数为0.1NA |
17.下列分子式表示的物质一定是纯净物的是( )
| A. | C5H10 | B. | 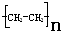 | C. | CH4O | D. | C2H4Cl2 |
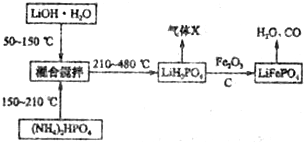

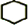 ,名称是环己烷
,名称是环己烷 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$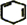 +2NaBr+2H2O.
+2NaBr+2H2O.