题目内容
6.下列指定反应的离子方程式正确的是( )| A. | FeO溶于稀硝酸:FeO+2H+═Fe2++H2O | |
| B. | Al2(SO4)3溶液中加入过量Ba(OH)2溶液:Al3++4OH-═AlO2-+2H2O | |
| C. | 漂白粉溶液中通入少量CO2:2ClO-+H2O+CO2═2HClO+CO32- | |
| D. | 等物质的量的NO和NO2同时被NaOH溶液吸收:NO+NO2+2OH-═2NO2-+H2O |
分析 A.稀硝酸具有强氧化性,能够将亚铁离子氧化成铁离子;
B.漏掉了钡离子与硫酸根离子生成硫酸钡沉淀的反应;
C.碳酸氢根离子的酸性小于次氯酸,二者反应生成碳酸氢根离子;
D.二氧化氮、一氧化氮与氢氧化钠溶液反应生成亚硝酸钠.
解答 解:A.氧化亚铁溶于稀硝酸,反应生成硝酸铁、NO气体和水,正确的离子方程式为:3FeO+NO3-+10H+═3Fe3++5H2O+NO↑,故A错误;
B.Al2(SO4)3溶液中加入过量Ba(OH)2溶液,反应生成硫酸钡沉淀和偏铝酸根离子,正确的离子方程式为:2Al3++3SO42-+3Ba2++8OH--=2AlO2-+4H2O+3BaSO4↓,故B错误;
C.漂白粉溶液中通入少量CO2,反应生成次氯酸和碳酸氢根离子,正确的离子方程式为:ClO-+H2O+CO2═HClO+HCO3-,故C错误;
D.等物质的量的NO和NO2同时被NaOH溶液吸收,反应的化学方程式为:NO+NO2+2OH-═2NO2-+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
13.设NA为阿伏伽德罗常数的值,则1molCu与足量的S完全反应,转移的电子数为( )
| A. | NA | B. | 1.5NA | C. | 2NA | D. | 不能确定 |
17.化学与生活密切相关,下列叙述与盐类水解无关的是( )
| A. | 久置的Na2S溶液可闻到臭鸡蛋气昧 | |
| B. | 利用FeCl3溶液腐蚀铜电路板 | |
| C. | 用NaHCO3和Al2(SO4)3溶液可以制作泡沫灭火剂 | |
| D. | 向煮沸的蒸馏水中滴加饱和FeCl3溶液制取Fe(OH)3胶体 |
14.下列实验的原理用离子方程式表示正确的是( )
| A. | 向用NaHSO4溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| B. | NaHSO4为离子化合物在熔融状态下能导电:NaHSO4=Na++H++SO42- | |
| C. | FeCl3腐蚀铜制印刷电路板:Fe3++Cu=Fe2++Cu2+ | |
| D. | NH4Cl溶液显酸性是因为NH4+发生水解:NH4++2H2O?NH3•H2O+H3O+ |
11.下列说法正确的是( )
| A. | 由电子定向移动而导电的物质不一定是金属 | |
| B. | 熔融态的NaHSO4能导电,则中只含有离子键 | |
| C. | HF的沸点高于HCl是因为F的非金属性比Cl强 | |
| D. | 足球烯(C60)和金刚石均为原子晶体,熔化时破坏共价键 |
3.将下列物质按酸、碱、盐分类排列,正确的是( )
| A. | 硫酸、纯碱、食盐 | B. | 硝酸、烧碱、胆矾 | ||
| C. | 碳酸、石灰石、蔗糖 | D. | 磷酸、熟石灰、苛性钾 |

 .
. .
.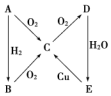 根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式:
根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式: