题目内容
6.下列说法正确的是( )| A. | 在常温下,浓硫酸不与铜反应,是因为铜被钝化 | |
| B. | 在BaC12溶液中通入SO2气体,溶液仍澄清,滴入3%过氧化氢溶液有白色沉淀 | |
| C. | 二氧化硫气体能用浓硫酸干燥,说明二氧化硫无还原性 | |
| D. | 硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫 |
分析 A.铜与浓硫酸不发生钝化反应;
B.过氧化氢可与二氧化硫发生氧化还原反应生成硫酸;
C.二氧化硫与硫酸不发生氧化还原反应;
D.硫和氧气反应只生成二氧化硫.
解答 解:A.铜与浓硫酸不发生钝化反应,加热条件下可反应生成二氧化硫和硫酸铜,故A错误;
B.二氧化硫与氯化钡不反应,在BaC12溶液中通入SO2气体,没有明显现象,但加入过氧化氢,过氧化氢可与二氧化硫发生氧化还原反应生成硫酸,与氯化钡反应生成硫酸钡沉淀,故B正确;
C.二氧化硫与硫酸S元素化合价相近,二者不发生氧化还原反应,故C错误;
D.硫和氧气反应只生成二氧化硫,二氧化硫在催化作用下可发生氧化还原反应,故D错误.
故选B.
点评 本题考查学生对元素化合物知识的熟悉程度,为高考常见题型,侧重考查学生的双基以及元素化合物知识的综合理解和运用,注意相关知识的积累,难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
16.短周期元素X、Y、Z、Q在元素周期表中的相对位置如图,地壳中含量最高的元素已包含其中.回答下列问题:
(1)Q在元素周期表中的位置是第二周期VIA族.X离子的结构示意图为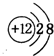 .
.
(2)下列选项中,能证明元素非金属性Z强于Y的是C.
A.反应中,Y原子得到的电子数比Z原子得到的电子数多
B.最高正价,Z比Y的高
C.最高价氧化物的水化物酸性:Z>Y
(3)ZQ2是国际公认高效安全杀菌消毒剂,已知ZQ2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ZQ2被还原为Z-,该反应的离子方程式为5Mn2++2ClO2+6H2O=5MnO2↓+2Cl-+12H+.
(4)H元素与Y形成的化合物中二者的质量之比是1:3,已知常温下4g该化合物完全燃烧并恢复到原来温度时放出222.6kJ热量,则表示该化合物燃烧热的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.4kJ/mol.
(5)表中X的最高价氧化物对应水化物的化学式为X(OH)n,在25℃时,其饱和溶液能使酚酞试液变红,则其饱和溶液中的pH=10.3(已知:25℃,Ksp[X(OH)n]=4.0×l0-12;lg5=0.7).
| Y | Q | ||||
| X | Z |
 .
.(2)下列选项中,能证明元素非金属性Z强于Y的是C.
A.反应中,Y原子得到的电子数比Z原子得到的电子数多
B.最高正价,Z比Y的高
C.最高价氧化物的水化物酸性:Z>Y
(3)ZQ2是国际公认高效安全杀菌消毒剂,已知ZQ2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ZQ2被还原为Z-,该反应的离子方程式为5Mn2++2ClO2+6H2O=5MnO2↓+2Cl-+12H+.
(4)H元素与Y形成的化合物中二者的质量之比是1:3,已知常温下4g该化合物完全燃烧并恢复到原来温度时放出222.6kJ热量,则表示该化合物燃烧热的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.4kJ/mol.
(5)表中X的最高价氧化物对应水化物的化学式为X(OH)n,在25℃时,其饱和溶液能使酚酞试液变红,则其饱和溶液中的pH=10.3(已知:25℃,Ksp[X(OH)n]=4.0×l0-12;lg5=0.7).
17.下列叙述正确的是( )
| A. | 用惰性电极电解某溶液时,若两极分别只有H2和O2生成,电解一段时间后,该溶液的浓度可能减小 | |
| B. | 电解精炼铜时,电解质溶液中铜离子浓度可能减小 | |
| C. | 原电池工作时,溶液中的阳离子向负极移动 | |
| D. | 要使电解后的CuSO4溶液复原,可向其中加人Cu(OH)2固体 |
1.有关化学用语正确的是( )
| A. | 乙炔的最简式为CH | |
| B. | 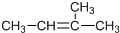 名称为顺-2甲基2丁烯 名称为顺-2甲基2丁烯 | |
| C. | 四氯化碳的电子式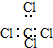 | |
| D. | 1,2-二溴乙烷的结构简式为C2H4Br2 |
18.将ag Fe2O3、Al2O3样品溶解在过量的200mL 0.05mol/L的硫酸溶液中然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
| A. | 0.1 mol•L-1 | B. | 0.2 mol•L-1 | C. | 0.4 mol•L-1 | D. | 0.8 mol•L-1 |
15.NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 0.1 mol丙烯酸中含有双键的数目为0.1NA | |
| B. | 常温常压下,Cu、Zn、稀硫酸构成的原电池中,正极产生1.12 L H2时,转移的电子数应为0.1NA | |
| C. | 一定条件下定容容器中充入3molH2(g)和1 mol N2(g)发生反应:H2(g)+N2(g)?2NH3 (g);△H=-QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.75 NA | |
| D. | 在50 g质量分数为46%的乙醇水溶液中,含有的氢原子总数为6NA |
16.以下实验或操作不能达到目的是( )
| A. | 除去乙烷中乙烯的方法是将气体通过足量的酸性KMnO4溶液 | |
| B. | 向2mL2%的硝酸银溶液中滴加2%的稀氨水至沉淀恰好溶解即得到银氨溶液 | |
| C. | 分别将去膜的镁条和铝片投入等浓度的稀盐酸中,通过观察实验现象判断其金属性强弱 | |
| D. | 在淀粉溶液中加入少量稀硫酸,加热4~5min,冷却后加入新制的氢氧化铜浊液并加热至沸腾,根据现象判断淀粉是否水解 |