题目内容
1.同周期元素X、Y、Z,其最高价氧化物对应的水化物是HXO4、H2YO4、H3ZO4,则下列判断正确的是( )| A. | 酸性:HXO4<H2Y O4<H3ZO4 | B. | 气态氢化物的稳定性:X<Y<Z | ||
| C. | 非金属性:X>Y>Z | D. | 元素负化合价的绝对值:X>Y>Z |
分析 同周期元素X、Y、Z,其最高价氧化物对应的水化物是HXO4、H2YO4、H3ZO4,可知X、Y、Z的最高正价分别为+7、+6、+5,则非金属性X>Y>Z,然后结合元素周期律来解答.
解答 解:同周期元素X、Y、Z,其最高价氧化物对应的水化物是HXO4、H2YO4、H3ZO4,可知X、Y、Z的最高正价分别为+7、+6、+5,则非金属性X>Y>Z,
A.非金属性越强,对应最高价含氧酸的酸性越强,则酸性:HXO4>H2YO4>H3ZO4,故A错误;
B.非金属性越强,对应氢化物越稳定,则气态氢化物的稳定性:X>Y>Z,故B错误;
C.由上述分析可知,非金属性:X>Y>Z,故C正确;
D.X、Y、Z的最高正价分别为+7、+6、+5,元素负化合价的绝对值:X<Y<Z,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握同周期元素对应的最高价含氧酸与非金属性的关系为解答的关键,侧重分析与应用能力的考查,注意元素周期律的应用,题目难度不大.

练习册系列答案
相关题目
11.下列说法中正确的是( )
| A. | 锗的第一电离能高于碳而电负性低于碳 | |
| B. | 乙烯分子中,只有一个碳碳π键,四个碳氢σ键 | |
| C. | 在铁制品上镀铜时,镀件为阳极,铜盐溶液为电镀液 | |
| D. | 甲醇分子内的O-C-H键角小于甲醛分子内O-C-H键角 |
9.化学是一门以实验为基础的自然科学,通过实验可以得知物质的组成、结构、性质及其变化规律.下列通过实验得出的结论正确的是( )
| A. | 天然气能在氧气中燃烧,说明氧气具有可燃性 | |
| B. | 水通电分解时生成氢气和氧气,说明水是由氢气和氧气组成 | |
| C. | 将石蕊试液滴入稀硫酸中溶液显红色,说明石蕊试液能使酸变红 | |
| D. | 通过在显微镜下观察木炭,得知木炭具有疏松多孔的结构 |
16.下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 银氨溶液:Na+、K+、NO3-、NH3•H2O | |
| B. | 存在Fe2+的溶液中:Mg2+、SO42-、ClO-、Na+ | |
| C. | 氢氧化铁胶体:H+、K+、S2-、Br- | |
| D. | 高锰酸钾溶液:H+、Na+、SO42-、葡萄糖分子 |
10.下列六种有机物:①2-甲基丁烷 ②2,2-二甲基丙烷 ③丙烷 ④戊烷 ⑤2-甲基丙烷 ⑥乙醇,按它们的沸点由高到低的顺序排列为( )
| A. | ①②③④⑤⑥ | B. | ②③④⑤⑥① | C. | ④⑤⑥②①③ | D. | ⑥④①②⑤③ |
11.下列反应的离子方程式正确的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ | |
| B. | 铁粉加入三氯化铁溶液中:2Fe+Fe3+=3Fe2+ | |
| C. | AlCl3溶液中加入过量氨水:Al3++4OH-→AlO2-+2H2O | |
| D. | FeCl2溶液中加入氯水:Cl2+2 Fe2+=2 Fe3++2Cl- |
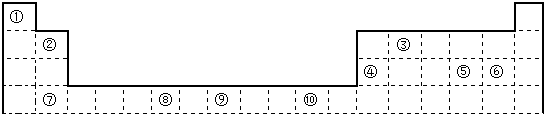
 .
. ;⑥和⑦形成的化合物电子式为
;⑥和⑦形成的化合物电子式为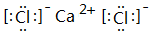 .③和⑥形成的化合物晶体类型为分子晶体.元素①的4个原子与元素③的2个原子形成的分子中含有σ键的数目为5,π键数目为1.
.③和⑥形成的化合物晶体类型为分子晶体.元素①的4个原子与元素③的2个原子形成的分子中含有σ键的数目为5,π键数目为1.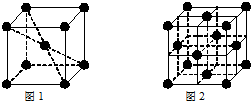
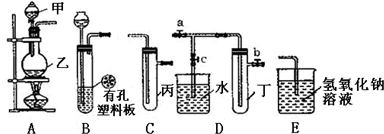
 ;用E的氧化物和氯化物都能干燥的气体有d
;用E的氧化物和氯化物都能干燥的气体有d