题目内容
5.已知某氢氧化物M(OH)2的溶度积常数为3.2×10-17,则M(OH)2在水中的溶解度为( )| A. | 2.0×10-6mol/L | B. | 3.2×10-6mol/L | C. | 2.0×10-9mol/L | D. | 3.2×10-9mol/L |
分析 设M(OH)2的浓度为x,则c(M2+)=x,c(OH-)=2x,利用Ksp=c(M2+)×c2(OH-)=4x3解答该题.
解答 解:设M(OH)2的浓度为x,则c(M2+)=x,c(OH-)=2x,利用Ksp=c(M2+)×c2(OH-)=4x3,即4x3=3.2×10-17mol/L=2.0×10-6mol/L,
故选A.
点评 本题考查了Ksp的有关计算,为高频考点,侧重于学生的分析、计算能力的考查,要注意溶液中离子浓度的关系,难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
10.某温度下,在一个2L的密闭容器中,加入4mol A和2mol B进行如下反应:3A(g)+2B(g)?4C(?)+2D(?).反应一段时间后达到平衡,测得生成1.6mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
| A. | 增加C,B的平衡转化率不变 | |
| B. | 此时,B的平衡转化率是35% | |
| C. | 增大该体系的压强,平衡向右移动,化学平衡常数增大 | |
| D. | 该反应的化学平衡常数表达式是K=$\frac{{c}^{4}(C){c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$ |
17.W、X、Y、Z均为原子序数依次增大的短周期主族元素,W、X、Y处于同一周期,W元素形成的化合物种类最多,W和Y族序数之和为X族序数的2倍,Z的最高价氧化物对应的水化物既能溶于酸又能溶于碱,下列说法中正确的是( )
| A. | 简单气态氢化物沸点Y>X>W | |
| B. | 原子半径Z>Y>X>W | |
| C. | Y元素可能位于第二周期第ⅦA族 | |
| D. | Y元素与其它三种元素均可形成多种化合物 |
14.下列反应中,水只作氧化剂的是( )
| A. | C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 | B. | Na2O+H2O═2NaOH | ||
| C. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |
15.将BaCl2溶液加入某无色溶液后,生成白色沉淀,再加入稀HNO3,则沉淀不溶解,下列说法正确的是( )
| A. | 一定存在Ag+ | B. | 一定存在CO32- | C. | 一定存在SO42- | D. | 以上说法都不对 |
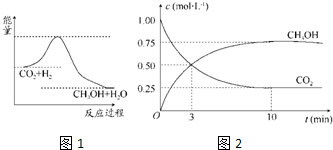
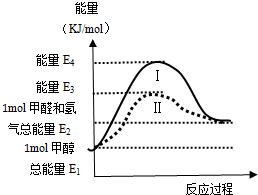 甲醇是重要的化工原料,气态甲醇催化脱氢制备甲醛转化的能量关系如图所示.
甲醇是重要的化工原料,气态甲醇催化脱氢制备甲醛转化的能量关系如图所示.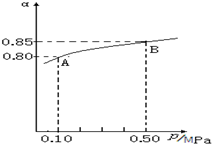 SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一.
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一.