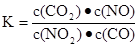题目内容
一定条件下,某反应的化学方程式为:CO2+NO?NO2+CO,下列说法正确的是( )
分析:A、升温增大反应速率,正逆反应速率都增大,增大程度不同;
B、反应是气体体积不变的反应,压缩容器体积压强增大,平衡不动,但物质浓度增大,红棕色二氧化氮气体颜色加深;
C、依据平衡常数的概念分析判断,平衡常数是生成物平衡浓度幂次方乘积除以反应物平衡浓度的幂次方乘积;
D、恒容时,升高温度,混合气体的颜色加深,二氧化氮是红棕色气体,说明平衡正向进行,正反应方向是吸热反应.
B、反应是气体体积不变的反应,压缩容器体积压强增大,平衡不动,但物质浓度增大,红棕色二氧化氮气体颜色加深;
C、依据平衡常数的概念分析判断,平衡常数是生成物平衡浓度幂次方乘积除以反应物平衡浓度的幂次方乘积;
D、恒容时,升高温度,混合气体的颜色加深,二氧化氮是红棕色气体,说明平衡正向进行,正反应方向是吸热反应.
解答:解:A、升温增大反应速率,正逆反应速率都增大,增大程度不同,故A错误;
B、反应是气体体积不变的反应,压缩容器体积压强增大,平衡不动,但物质浓度增大,红棕色二氧化氮气体颜色加深,故B正确;
C、依据平衡常数的概念分析判断,平衡常数是生成物平衡浓度幂次方乘积除以反应物平衡浓度的幂次方乘积,选项中是反应物浓度除以生成物浓度,故C错误;
D、恒容时,升高温度,混合气体的颜色加深,二氧化氮是红棕色气体,说明平衡正向进行,依据平衡移动原理可知,正反应方向是吸热反应,逆反应方向是放热反应,故D正确;
故选:BD.
B、反应是气体体积不变的反应,压缩容器体积压强增大,平衡不动,但物质浓度增大,红棕色二氧化氮气体颜色加深,故B正确;
C、依据平衡常数的概念分析判断,平衡常数是生成物平衡浓度幂次方乘积除以反应物平衡浓度的幂次方乘积,选项中是反应物浓度除以生成物浓度,故C错误;
D、恒容时,升高温度,混合气体的颜色加深,二氧化氮是红棕色气体,说明平衡正向进行,依据平衡移动原理可知,正反应方向是吸热反应,逆反应方向是放热反应,故D正确;
故选:BD.
点评:本题考查了化学平衡影响因素的分析判断,化学平衡移动原理的理解应用和反应特征分析是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
|
一定条件下,某反应的化学方程式为:CO2+NO | |
| [ ] | |
A. |
升高温度,正反应速率增大,逆反应速率减少 |
B. |
恒温时,压缩容器的体积,颜色加深,因平衡左移 |
C. |
达到平衡,其平衡常数为K= |
D. |
恒容时,升高温度,混合气体的颜色加深,该反应的焓变为正值 |
一定条件下,某反应的化学方程式为:CO2+NO  NO2+CO ,下列说法正确的是( )
NO2+CO ,下列说法正确的是( )
| A.升高温度,正反应速率增大,逆反应速率减少 |
| B.恒温时,压缩容器的体积,颜色加深,因平衡左移 |
C.达到平衡,其平衡常数为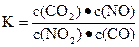 |
| D.恒容时,升高温度,混合气体的颜色加深,该反应的焓变为正值 |
 NO2+CO ,下列说法正确的是( )
NO2+CO ,下列说法正确的是( )