��Ŀ����
6����25��ʱ����ʯī�缫���2.0L2.5mol/LCuSO4��Һ��5min����һ��ʯī�缫����6.4gCu���ɣ��Իش���1����ⷴӦ�����ӷ���ʽΪ2CuSO4+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+O2��+2H2SO4��
��2����������Һ��������䣬�������Һ��pHΪ1��
��3����Ҫ����Һ�ָ�������ǰһ�����������CuO��CuCO3�����ѧʽ��
��4�����顢����������������Һ��ɵ�ȼ�ϵ�أ������ķ�ӦʽΪCH4-8e-+10OH-=CO32-+7H2O�����ɸ�ȼ�ϵ��Ϊ������ⷴӦ�ṩ��Դ��������������̣�����������CH40.4g����Ӧ��ת�Ƶĵ�����Ϊ0.2mol��
���� ��25��ʱ����ʯī�缫���2.0 L2.5mol/LCuSO4��Һ��Cu2+���ʵ���Ϊ2��2.5=5mol��5min����һ��ʯī�缫����6.4 g Cu�������ʵ���Ϊ0.1mol��
��1�����CuSO4��Һ��ʵ���ǵ���κ�ˮ�����ݵ缫��Ӧ��д��ⷽ��ʽ��
��2�����ݵ缫��Ӧ�����غ㣬����ͭ���ʵ���Ϊ0.1mol������ת��Ϊ0.2mol��
������ӦΪ4OH--4e-�T2H2O+O2��
0.2mol 0.2mol 0.05mol
������ӦΪ2Cu2++4e-�T2Cu
0.1mol 0.2mol 0.1mol
���Ե������е���ת��Ϊ0.2mol��
�������������=0.05mol��22.4L/mol=1.12L��
��Һ��PH�ļ����������ˮ������������Ӻ������������غ㣬��������������0.2mol����Һ������������0.2mol��c��H+��=$\frac{0.2mol}{2L}$=0.1mol/L��pH=-lgC��H+��=1��
��3������ȱʲô��ʲô����ϵ�ⷽ��ʽ�������Ҫ��������ʣ�
��4�����ݸ����ϵĵ缫��Ӧʽ���ڵ�ص��ܷ�Ӧʽ-���������ĵ缫����ʽ�����ݵ�ʧ�����غ���㣮
��� �⣺��25��ʱ����ʯī�缫���2.0 L2.5mol/LCuSO4��Һ��Cu2+���ʵ���Ϊ2��2.5=5mol��5min����һ��ʯī�缫����6.4 g Cu�������ʵ���Ϊ0.1mol��
��1���������ͭʱ�����������������ŵ磬��������ͭ���ӷŵ磬������Ӧ��2Cu2++4e-��2Cu��������Ӧ��4OH-��4e-+2H2O+O2�������ʱ��Ӧ�������ӷ���ʽΪ��2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+4H++O2�����ʴ�Ϊ��2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+4H++O2����
��2�����ݵ缫��Ӧ�����غ㣬����ͭ���ʵ���Ϊ0.1mol������ת��Ϊ0.2mol��
������ӦΪ4OH--4e-�T2H2O+O2��
0.2mol 0.2mol 0.05mol
������ӦΪ2Cu2++4e-�T2Cu
0.1mol 0.2mol 0.1mol
���Ե������е���ת��Ϊ0.2mol��
�������������=0.05mol��22.4L/mol=1.12L��
��������������0.2mol����Һ������������0.2mol��c��H+��=$\frac{0.2mol}{2L}$=0.1mol/L��pH=-lgc��H+��=1��
�ʴ�Ϊ��1��
��3�����ݵ������ӷ���ʽ2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+O2��+4H+�����������˽���ͭ���������ų�������Ҫ����Һ��ԭ������� CuO��CuCO3���ʴ�Ϊ��CuO��CuCO3��
��4�������ϵĵ缫��Ӧʽ���ڵ�ص��ܷ�Ӧʽ-���������ĵ缫����ʽ���Լ��顢����������������ҺΪԭ�ϣ����Ե缫�ɹ���ȼ�ϵ�أ�������ӦΪ��3O2+12H2O+12e-=12OH-���ܷ�ӦʽΪ��CH4+2O2+2OH-=CO32-+3H2O����ʽ�����������ӦΪ��CH4-8e-+10OH-=CO32-+7H2O����������������0.1molͭ��ת��0.2mol���ӣ������CH4-8e-+10OH-=CO32-+7H2O����������CH4 Ϊ$\frac{0.2}{8}$��16=0.4g����Ӧ��ת�Ƶĵ�����Ϊ0.2mol��
�ʴ�Ϊ��CH4-8e-+10OH-=CO32-+7H2O��0.4g��0.2mol��
���� ���⿼���˵��ԭ����Ӧ�ã��缫��Ӧ���жϣ��缫��Ӧ����д�����������غ�ļ���Ӧ�ã�ȼ�ϵ�ص�ԭ�������ͼ���Ӧ�ã�

| A�� | ���������м���������ˮ��Һ�����ȣ�Ȼ�����������Һ������Ԫ�� | |
| B�� | ����м����ˮ����������屽 | |
| C�� | �ڱ�����Һ�е�������ϡ��ˮ���ְ�ɫ���� | |
| D�� | ��ͭ˿�ھƾ����ϼ��Ⱥ�����������ˮ�Ҵ��У�ͭ˿�ָ���ԭ���ĺ�ɫ |
| A�� | CH3Cl | B�� | CH3CHBrCH3 | C�� |  | D�� |  |
| A�� | ��ˮ | B�� | FeCl3��Һ | C�� | ����KMnO4��Һ | D�� | AgNO3��Һ |
| A�� | ±�� | B�� | ��������Ԫ�� | C�� | �ڶ�����Ԫ�� | D�� | �ڢ�A��Ԫ�� |
| A�� | Һ�� | B�� | ���� | C�� | ʳ��ˮ | D�� | �Ȼ��ƾ��� |
 �Թ�ҵ��ˮ��������ˮ���д����Ƿ�ֹˮ����Ⱦ������ˮ�ʵ���Ҫ��ʩ��
�Թ�ҵ��ˮ��������ˮ���д����Ƿ�ֹˮ����Ⱦ������ˮ�ʵ���Ҫ��ʩ��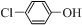 ���ķ�ˮ����ͨ�����������س�ȥ����ԭ����ͼ��ʾ����B�ǵ�صĸ��������������������A���ĵ缫��ӦʽΪ
���ķ�ˮ����ͨ�����������س�ȥ����ԭ����ͼ��ʾ����B�ǵ�صĸ��������������������A���ĵ缫��ӦʽΪ -OH+Cl-��
-OH+Cl-�� ��1���۲�ͼA��B��C���ش��������⣺
��1���۲�ͼA��B��C���ش��������⣺