题目内容
下列反应中属于氧化还原反应,伹水既不作氧化剂又不作还原剂的是( )
| A、SO3+H2O=H2SO4 |
| B、Cl2+H2O=HCl+HClO |
| C、2F2+2H2O=4HF+O2 |
| D、2Na+2H2O=2NaOH+H2↑ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应中含元素的化合价变化,为氧化还原反应,但水中H、O元素的化合价不变,则水既不作氧化剂又不作还原剂,以此来解答.
解答:
解:A.SO3+H2O=H2SO4中没有元素的化合价的变化,不属于氧化还原反应,故A不选;
B.Cl2+H2O=HCl+HClO只有Cl元素的化合价变化,为水既不作氧化剂又不作还原剂的氧化还原反应,故B选;
C.2F2+2H2O=4HF+O2,水中O元素的化合价升高,F元素的化合价降低,属于氧化还原反应,水为还原剂,故C不选;
D.2Na+2H2O=2NaOH+H2↑Na元素的化合价升高,水中H元素的化合价降低,属于氧化还原反应,水为氧化剂,故D不选;
故选B.
B.Cl2+H2O=HCl+HClO只有Cl元素的化合价变化,为水既不作氧化剂又不作还原剂的氧化还原反应,故B选;
C.2F2+2H2O=4HF+O2,水中O元素的化合价升高,F元素的化合价降低,属于氧化还原反应,水为还原剂,故C不选;
D.2Na+2H2O=2NaOH+H2↑Na元素的化合价升高,水中H元素的化合价降低,属于氧化还原反应,水为氧化剂,故D不选;
故选B.
点评:本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断的考查,题目难度不大.

练习册系列答案
相关题目
 联合国气候变化大会于2010年12月召开,焦点议题之一是发展“低碳经济,节能减排”,减少温室气体排放.你认为下列做法中,不能有效减少空气中CO2含量的是( )
联合国气候变化大会于2010年12月召开,焦点议题之一是发展“低碳经济,节能减排”,减少温室气体排放.你认为下列做法中,不能有效减少空气中CO2含量的是( )| A、开发利用太阳能、风能、生物能、海洋能等清洁能源 |
| B、使用节能产品,推广节能环保汽车 |
| C、植树造林,增加森林植被面积 |
| D、用脱硫处理的煤代替原煤作燃料 |
在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是( )
| A、pH=3的醋酸和pH=11氢氧化钠溶液 |
| B、pH=2的硫酸和pH=12的氢氧化钠溶液 |
| C、pH=3的盐酸和pH=11的氨水 |
| D、pH=2的硝酸和pH=12的氢氧化钠溶液 |
盐酸能发生下列反应:①Zn+2HCl═ZnCl2+H2↑②2HCl+CuO═CuCl2+H2O ③MnO2+4HCl═MnCl2+Cl2↑+2H2O,因此盐酸具有的性质是( )
| A、只有酸性 |
| B、只有氧化性 |
| C、只有还原性 |
| D、以上三种均具有 |
下列反应的化学方程式(或离子方程式)书写正确的是( )
A、实验室制乙烯:CH3CH2OH
| |||
| B、苯酚钠溶液通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |||
C、甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH-
| |||
D、工业制聚乙烯:nCH2=CH2
 |
下列物质中,熔融状态不能导电的电解质是( )
| A、Na2SO4 |
| B、NaOH |
| C、C2H5OH |
| D、H2SO4 |
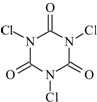 三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂.
三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂.