题目内容
7.硫酸的消费量是衡量一个国家化工生产水平的重要标,而在硫酸的生产中,最关键的一步反应为:SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g).(1)一定条件下,SO2与O2反应10min后,若SO2和SO3物质的量浓度分别为1mol/L和3mol/L,则SO2起始物质的量浓度为4mol/L;10min生成SO3的化学反应速率为0.3mol/(L•min).
(2)下列关于该反应的说法正确的是AC.
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3.
分析 (1)根据初始时加入的SO2和O2,反应10min后,SO3物质的量浓度3mol/L,则反应生成了SO33mol/L,根据转化量之比=化学计量数之比,则转化的SO2为3mol,由反应物初始量=转化量+剩余的量,计算出SO2起始物质的量浓度,根据v=$\frac{△c}{△t}$计算v(SO3);
(2)根据外界条件对反应速率的影响及可逆反应不可能完全转化.
解答 解:(1)根据初始时加入的SO2和O2,反应10min后,SO3物质的量浓度3mol/L,则反应生成了SO33mol/L,根据转化量之比=化学计量数之比,则转化的SO2为3mol/L,由反应物初始量=转化量+剩余的量,计算出SO2起始物质的量浓度=1mol/L+3mol/L=4mol/L,根据v=$\frac{△c}{△t}$,v(SO3)=$\frac{3mol/L}{10min}$=0.3mol/(L•min),
故答案为:4mol/L;0.3mol/(L•min);
(2)根据外界条件对反应速率的影响及可逆反应不可能完全转化,
A.增加O2的浓度能加快反应速率,故A正确;
B.降低体系温度会减慢反应速率,故B错误;
C.使用催化剂能加快反应速率,故C正确;
D.可逆反应不可能完全转化,故D错误,
故选AC.
点评 本题主要考查化学反应速率的基本计算及外界条件对化学反应速率的影响,题目难度不大.

练习册系列答案
相关题目
17.短周期主族元素X、Y、Z、W在元素周期表中的相对位置如下图所示.已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是( )
| X | ||||
| Y | Z | W |
| A. | X分别与Y、Z形成的化合物中化学键类型相同 | |
| B. | Z的最高价氧化物的对应水化物酸性比W的强 | |
| C. | X的简单气态氢化物的稳定性比W的弱 | |
| D. | Y是第三周期第ⅡA族元素 |
18.表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,X与Y的原子序数之和为Z与W原子序数之和的$\frac{2}{3}$.下列说法正确的是( )
| X | |||
| Y | Z | W | |
| T |
| A. | 化合物YX2、ZX2化学键类型和晶体类型均相同 | |
| B. | Z、W、T三种元素最高价氧化物的水化物的酸性依次增强 | |
| C. | 五种元素中,只有T是金属元素 | |
| D. | Mg在一定条件下可以和YX2发生反应生成Y单质 |
15.断肠草是葫蔓藤科植物葫蔓藤,其中的毒素很多.以下是分离出来的四种毒素的结构简式:
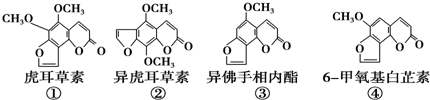
下列推断正确的是( )

下列推断正确的是( )
| A. | ②、③互为同系物 | |
| B. | ①、③各1mol与足量氢氧化钠溶液反应时均消耗3molNaOH | |
| C. | 等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者少 | |
| D. | ③、④互为同分异构体,它们各1mol均能与5molH2加成 |
12.Li-Al/FeS电池具有大容量、小污染、低成本及原料储备丰富等优点,电池总反应式为:4Li+FeS2$?_{充电}^{放电}$2Li2S+Fe,下列有关该电池的说法正确的是( )
| A. | 放电时,锂铝合金作负极,Li+向负极移动 | |
| B. | 充电时,阴极的电极反应式为:Fe+2Li2S-4e-=4Li++FeS2 | |
| C. | 该电池可用LiCl水溶液作电解质溶液 | |
| D. | 以Al作阳极,FeS为阴极,LiCl-KCl低共熔混合物为电解质进行电解,可以制得FeS2 |

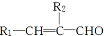 +H2O
+H2O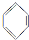 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$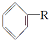 +HCl
+HCl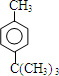 ;
;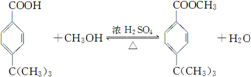 ;
;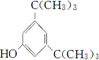 .
. .
.