题目内容
2.将盛有N2和NO2混合气体的试管倒立与水中,经过足够长的时间,试管内的气体体积缩小为原来的三分之二,则混合气体中N2和NO2的体积比是( )| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
分析 设原混合物的体积为1L,则反应后气体为$\frac{2}{3}$L,发生反应3NO2+H2O=2HNO3+NO,利用差量法计算V(NO2),进而计算V(N2),以此解答该题.
解答 解:设原混合物的体积为1L,反应后气体为$\frac{2}{3}$L,则:
3NO2+H2O=2HNO3+NO 体积减少
3 1 3-1=2
V(NO2) 1L-$\frac{2}{3}$L=$\frac{1}{3}$L
所以,V(NO2)=0.5L,则V(N2)=1L-0.5L=0.5L
故V(N2):V(NO2)=0.5L:0.5L=1:1,
故选A.
点评 本题考查混合物的有关计算,为高频考点,侧重考查学生的分析能力和计算能力,难度中等,利用赋值法可以减少计算量,注意差量法的应用.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
10.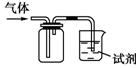 如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是( )
如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是( )
 如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是( )
如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是( )| 选项 | 试剂 | 现象 | 结论 |
| A | 酸性KMnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | 品红溶液 | 溶液褪色 | SO2有漂白性 |
| C | NaOH溶液 | 无明显现象 | SO2与NaOH溶液不反应 |
| D | 紫色石蕊试液 | 溶液变红色后不褪色 | SO2有酸性,没有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
17.在含有多个电子的原子里,能量高的电子通常是在( )
| A. | 离核近的区域运动 | B. | 离核远的区域运动 | ||
| C. | 无法确定运动区域离核远近 | D. | 化学变化中较难失去 |
7.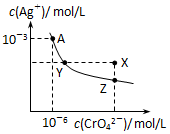 已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | T℃时Ag2CrO4的Ksp=2×10-12 | |
| B. | 浓度均为2×10-5mol/LAgNO3溶液与NaCl溶液等体积混合没有沉淀生成 | |
| C. | 在饱和Ag2CrO4溶液中加入K2CrO4固体可使溶液由Y点到X点 | |
| D. | 保持温度T℃不变,Ag2CrO4溶液长时间放置可使溶液由X点到Z点 |
14.下列物质中不属于卤代烃的是( )
| A. | C6H5Cl | B. | CH2=CHCl | C. | CH3COCl | D. | CH2Br2 |
11.下列物质中能使酸性KMnO4溶液褪色,也能使溴水褪色的是( )
| A. | 2,3-二甲基-2-己烯 | B. | 苯 | ||
| C. | 已烷 | D. | 异丙苯 | ||
| E. | 环戊烷 |