题目内容
下列反应的离子方程式不正确的是( )
| A、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氢氧化钠溶液与盐酸反应:OH-+H+=H2O |
| C、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
| D、氯化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
考点:离子方程式的书写
专题:
分析:A.反应生成氯化亚铁和氢气;
B.反应生成氯化钠和水;
C.反应生成盐酸和HClO;
D.反应生成硫酸钡和盐酸.
B.反应生成氯化钠和水;
C.反应生成盐酸和HClO;
D.反应生成硫酸钡和盐酸.
解答:
解:A.铁与稀盐酸反应的离子反应为Fe+2H+=Fe2++H2↑,故A错误;
B.氢氧化钠溶液与盐酸反应的离子反应为OH-+H+=H2O,故B正确;
C.氯气与水反应的离子反应为Cl2+H2O═H++Cl-+HClO,故C错误;
D.氯化钡溶液与稀硫酸反应的离子反应为Ba2++SO42-=BaSO4↓,故D正确;
故选AC.
B.氢氧化钠溶液与盐酸反应的离子反应为OH-+H+=H2O,故B正确;
C.氯气与水反应的离子反应为Cl2+H2O═H++Cl-+HClO,故C错误;
D.氯化钡溶液与稀硫酸反应的离子反应为Ba2++SO42-=BaSO4↓,故D正确;
故选AC.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,题目难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
 向盛有一定量浓度NaOH溶液的烧杯中通入一定量的CO2气体后得溶液M,向所得溶液M中逐滴加入稀盐酸至过量,并将溶液加热,产生气体与加入稀盐酸的物质的量的关系如图所示,则M中的主要溶质为( )
向盛有一定量浓度NaOH溶液的烧杯中通入一定量的CO2气体后得溶液M,向所得溶液M中逐滴加入稀盐酸至过量,并将溶液加热,产生气体与加入稀盐酸的物质的量的关系如图所示,则M中的主要溶质为( )| A、Na2CO3 |
| B、NaHCO3 |
| C、Na2CO3、NaOH |
| D、NaHCO3、NaOH |
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、10 g氖气中所含的原子数为NA |
| B、0.5 NA个Cl2分子的物质的量是3.01×1023mol |
| C、标准状况下,将22.4 L氯化氢气体溶于足量水中,溶液中含有的氯化氢分子数为NA |
| D、9 g水含有的电子数为5 NA |
下列有关化学用语使用正确的是( )
A、质量数为37的氯原子:
| ||
B、CH4Si的结构式: | ||
C、氨基的电子式: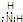 | ||
| D、Li+核外电子排布式 1s2 |
20世纪90年代,国际上提出了“预防污染”这一新概念.绿色化学是“预防污染”的基本手段.下列各项中属于绿色化学的是( )
| A、杜绝污染源 |
| B、减少有害物质 |
| C、治理污染点 |
| D、处理废弃物 |
元素及其化合物丰富了物质世界,下列说法正确的是( )
| A、铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象 |
| B、NaOH溶液和AlCl3溶液相互滴加的现象不同 |
| C、金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| D、Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与H2O发生反应 |
