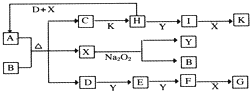
题目内容
用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、7.8 g Na2O2与足量潮湿的CO2反应,转移的电子数为0.1 NA |
| B、标准状况下2.24 L HCHO中含0.4 NA个原子 |
C、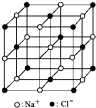 23.4 g NaCl晶体中含0.1 NA个如图所示结构单元 23.4 g NaCl晶体中含0.1 NA个如图所示结构单元 |
| D、电解精炼铜时转移0.1 NA个电子时,阳极溶解3.2 g铜 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、Na2O2与CO2的反应是歧化反应;
B、标况下,甲醛为气体;
C、根据图示得出如图所示的结构单元所表示的Na+和Cl-个数,然后根据n=
来计算;
D、在电解精炼时,阳极是粗铜,粗铜中含有杂质.
B、标况下,甲醛为气体;
C、根据图示得出如图所示的结构单元所表示的Na+和Cl-个数,然后根据n=
| m |
| M |
D、在电解精炼时,阳极是粗铜,粗铜中含有杂质.
解答:
解:A、7.8 g Na2O2的物质的量n=
=
=0.1mol,而Na2O2与CO2的反应是歧化反应:2Na2O2+2CO2=2Na2CO3+O2↑反应转移2mol电子,故0.1molNa2O2转移0.1mol电子,即0.1NA个,故A正确;
B、标准状况下,2.24 L HCHO的物质的量n=
=
=0.1mol,而1molHCHO含4mol原子,故0.1mol甲醛含0.4mol原子,个数为0.4 NA个,故B正确;
C、根据n=
可知23.4 g NaCl的物质的量n=
=0.4mol,而此结构单元中含有的Na+的个数为(1+12×
)即4个,含有的Cl-个数为(6×
+8×
)即4个;故0.4mlNaCl即0.1mol此结构单元,个数为0.1NA个,故C正确;
D、在电解精炼时,阳极是粗铜,粗铜中含有一些比铜活泼的杂质,在阳极优先于铜放电,故当转移0.1 NA个电子时,阳极溶解的铜少于3.2g,故D错误.
故选D.
| m |
| M |
| 7.8g |
| 78g/mol |
B、标准状况下,2.24 L HCHO的物质的量n=
| V |
| Vm |
| 2.24L |
| 22.4L/mol |
C、根据n=
| m |
| M |
| 23.4 |
| 58.5g/mol |
| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 8 |
D、在电解精炼时,阳极是粗铜,粗铜中含有一些比铜活泼的杂质,在阳极优先于铜放电,故当转移0.1 NA个电子时,阳极溶解的铜少于3.2g,故D错误.
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的运用和物质结构是关键,难度不大.

练习册系列答案
相关题目
下列说法中,不正确的是( )
| A、食醋中含有的醋酸外还含有氨基酸 |
| B、谷类中含有的淀粉 |
| C、牛瘦肉中富含纤维素 |
| D、天然气是混合物 |
下列反应属于吸热反应的是( )
| A、C6H12O6(葡萄糖)+6O2═6CO2+6H2O |
| B、CH3COOH+KOH═CH3COOK+H2O |
| C、所有高温条件下发生的反应 |
| D、破坏生成物全部化学键所需能量小于破坏反应物全部化学键的能量 |
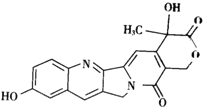 具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的就法错误的是( )
具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的就法错误的是( )| A、该物质属于有机物 |
| B、该物质不属于烃 |
| C、该物质完全燃烧后的产物只有CO2和H2O |
| D、该物质中既含有极性键又含有非极性键 |
下列物质的分子中,只含有极性共价键的是( )
| A、氯化镁 | B、单质碘 | C、乙烷 | D、水 |
NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、实验室以H2O2和MnO2为原料制取O2,每生成1mol O2转移2NA个电子 |
| B、标准状况下,0.5NA个H2O分子所占有的体积为11.2L |
| C、1mol 硫酸钾中阴离子所带电荷数为NA |
| D、18.0g NH4+中所含的质子数为10NA |
比较下列各组物质的沸点,正确的是( )
| A、乙醇>丙烷 |
| B、异戊烷>正戊烷 |
| C、1-丁烯>1-庚烯 |
| D、乙二醇>丙三醇 |
下列关于有机物的说法正确的是( )
| A、乙醇、乙烷和乙酸都可以与钠反应生成氢气 |
| B、乙醇可以被酸性重铬酸钾溶液直接氧化为乙酸 |
| C、乙烯使溴水和酸性高锰酸钾溶液褪色的反应均属于加成反应 |
| D、汽油、柴油和植物油都是碳氢化合物 |