题目内容
已知95℃时,水的离子积常数为1×10-12.在此温度下,将pH=8的NaOH溶液与pH=4的H2SO4溶液相混合,得到pH=7的混合溶液,则NaOH溶液与H2SO4溶液的体积比为 .
考点:pH的简单计算
专题:计算题,电离平衡与溶液的pH专题
分析:95℃时,水的离子积常数为1×10-12,Kw=c(OH-)×c(H+),PH=6时,溶液呈中性.pH=4的H2SO4溶液,c(H+)=1×10-4mol/L,pH=8的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=
mol/L=1×10-4mol/L,要使混合液的pH=7,溶液呈碱性,即氢氧化钠过量,混合溶液中氢氧根离子的物质的量浓度=
=10-5 mol/L.据此解答.
| 1×10-12 |
| 1×10-8 |
| 10-12 |
| 10-7 |
解答:
解:95℃时,水的离子积常数为1×10-12,Kw=c(OH-)×c(H+),PH=6时,溶液呈中性.
pH=4的H2SO4溶液,c(H+)=1×10-4mol/L,pH=8的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=
mol/L=1×10-4mol/L,设pH=4的H2SO4溶液XL和pH=8的NaOH溶液YL混合,混合液的pH=7,氢氧化钠过量,混合溶液中氢氧根离子的物质的量浓度=
=10-5mol/L,两种溶液混合后氢氧化钠的物质的量浓度:
=10-5mol/L,所以X:Y=9:11,
故答案为:11:9;
pH=4的H2SO4溶液,c(H+)=1×10-4mol/L,pH=8的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=
| 1×10-12 |
| 1×10-8 |
| 10-12 |
| 10-7 |
| 1×10-4×Y-1×10-4×X |
| X+Y |
故答案为:11:9;
点评:本题考查了混合溶液PH的计算,难度不大,注意该题中中性溶液的PH不等于7而是为6,能灵活运用水的离子积常数是解本题的关键.

练习册系列答案
相关题目
下列操作不能达到目的是( )
| A、将25g CuSO4?5H2O溶于100 mL蒸馏水中,配制100mol l.0 mol/LCuSO4溶液 |
| B、检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的红色石蕊试纸检验逸出的气体 |
| C、用加热分解的方法区分碳酸钠和碳酸氢钠两种固体 |
| D、用银氨溶液鉴别葡萄糖和蔗糖 |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:方案一:铜铝混合物
测定生成气体的体积方案二:铜铝混合物
测定剩余固体的质量下列有关判断中不正确的是( )
| 足量溶液A |
| 充分反应 |
| 足量溶液B |
| 充分反应 |
| A、溶液A和溶液B均可以是盐酸或NaOH溶液 |
| B、方案一可能产生氢气,方案二可能剩余铜 |
| C、若溶液B选用浓硝酸,测得铜的质量分数偏大 |
| D、实验室中方案Ⅱ更便于实施 |
下列各组实验中溶液最先变浑浊的是( )
| A、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度10℃ |
| B、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度10℃ |
| C、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度30℃ |
| D、0.2 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度30℃ |
对于可逆反应A(g)+B(g)?C(g)△H<0,下列图象正确的是( )
A、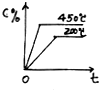 |
B、 |
C、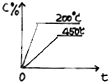 |
D、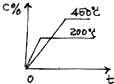 |
下列说法正确的是( )
| A、已知a g乙烯气体充分燃烧时生成1 mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-4b kJ?mol-1 | ||||
| B、已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ?mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | ||||
C、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)
| ||||
| D、已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5 kJ?mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ?mol-1,则C(s,金刚石)═C(s,石墨)△H=-1.5 kJ?mol-1 |
某烃的结构简式为 分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )
分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )
 分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )
分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )| A、4,5,3 |
| B、4,6,3 |
| C、2,4,5 |
| D、4,4,6 |