题目内容
用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
 A.25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA
A.25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA
 B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
 C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
 D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
C
【解析】
试题分析:A、25℃时,1.0L pH=13的Ba(OH)2溶液中氢氧根离子的浓度是0.1mol/L,则氢氧根离子的物质的量是0.1mol/L×1.0L=0.1mol,所以氢氧根离子数目是0.1NA,错误;B、氯气与氢氧化钠的反应中,氯气既是氧化剂又是还原剂,所以标准状况下2.24L的氯气的物质的量是0.1mol,与氢氧化钠溶液完全反应时,转移电子的物质的量是0.1mol,电子数是0.1NA,错误;C、乙烯和丁烯的最简式相同都是CH2,则21.0g的乙烯与丁烯的混合物中C原子的物质的量是21.0g/14g/mol=1.5mol,碳原子数目为1.5NA,正确;D、标准状况下甲醇不是气体,所以22.4L的甲醇的物质的量不是1mol,错误,答案选C。
考点:考查阿伏伽德罗常数的应用

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、烃分子中的碳原子与其他原子的结合方式一定是通过非极性键 | B、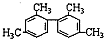 分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面 | C、聚乙烯能使溴水褪色 | D、软脂酸和油酸互为同系物 |
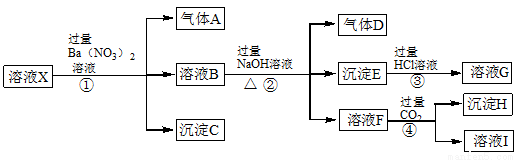
 2Cu+SO2反应制取粗铜,当有32gCu2S消耗时,电子转移数目是 。
2Cu+SO2反应制取粗铜,当有32gCu2S消耗时,电子转移数目是 。