题目内容
8.核内中子数为N的R2+,质量数为A,则n g它的氧化物中所含质子的物质的量是( )| A. | $\frac{n}{A+16}$(A-N+8)mol | B. | $\frac{n}{A+16}$(A-N+10)mol | C. | $\frac{n}{A}$ (A-N+2)mol | D. | $\frac{n}{A}$(A-N+6)mol |
分析 该离子的质子数=A-N,根据化合物中化合价的代数和为0知,该氧化物的化学式为RO,一个RO中质子数是A-N+8,先计算氧化物的物质的量,再根据质子的物质的量.
解答 解:根据化合物中化合价的代数和为0知,该氧化物的化学式为RO,该氧化物的物质的量=$\frac{ng}{(A+16)g/mol}$=$\frac{n}{A+16}$mol,
该离子的质子数=A-N,一个RO中质子数=A-N+8,
则ng它的氧化物中所含质子的物质的量=$\frac{n}{A+16}$mol×(A-N+8)=$\frac{n}{A+16}$(A-N+8)mol,
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确“数值上,原子的相对原子质量等于其质量数“是解本题的关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
16.有机物A是某种药物的中间体,其结构简式为: 关于有机物A的说法不正确的是( )
关于有机物A的说法不正确的是( )
 关于有机物A的说法不正确的是( )
关于有机物A的说法不正确的是( )| A. | A的分子式为C16H1403 | |
| B. | A可使酸性KMnO4溶液褪色和溴水褪色 | |
| C. | A苯环上的一氯代物同分异构体有2种 | |
| D. | A既可发生氧化反应和加成反应,又可以发生取代反应 |
3. (1)某元素原子的价电子构型为4s24p1,它属于第四周期ⅢA族,属p区元素.
(1)某元素原子的价电子构型为4s24p1,它属于第四周期ⅢA族,属p区元素.
(2)基态磷原子核外有15种运动状态不同的电子.
(3)CO的结构可表示为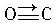 与CO结构最相似的分子是N2,这两种结构相似的分子中,分子的极性不相同(填“相同”或“不相同”).
与CO结构最相似的分子是N2,这两种结构相似的分子中,分子的极性不相同(填“相同”或“不相同”).
(4)实验证明:KCl、MgO、CaO三种晶体的结构与NaCl晶体的结构相似,已知NaCl、KCl、CaO晶体的晶格能数据如下表:
则KCl、MgO、CaO三种晶体的熔点从高到低的顺序是MgO>CaO>KCl.其中MgO晶体中一个Mg2+周围和它最近且等距离的Mg2+有12个.
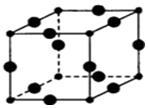
(5)Cu3N的晶胞结构如图,N3-的配位数为6,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为$\frac{103}{4{N}_{A}(a+b)^{3}}$g•cm-3.(阿伏加德罗常数用NA表示)
 (1)某元素原子的价电子构型为4s24p1,它属于第四周期ⅢA族,属p区元素.
(1)某元素原子的价电子构型为4s24p1,它属于第四周期ⅢA族,属p区元素.(2)基态磷原子核外有15种运动状态不同的电子.
(3)CO的结构可表示为
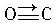 与CO结构最相似的分子是N2,这两种结构相似的分子中,分子的极性不相同(填“相同”或“不相同”).
与CO结构最相似的分子是N2,这两种结构相似的分子中,分子的极性不相同(填“相同”或“不相同”).(4)实验证明:KCl、MgO、CaO三种晶体的结构与NaCl晶体的结构相似,已知NaCl、KCl、CaO晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3 401 |
(5)Cu3N的晶胞结构如图,N3-的配位数为6,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为$\frac{103}{4{N}_{A}(a+b)^{3}}$g•cm-3.(阿伏加德罗常数用NA表示)
4.一定量的甲烷燃烧后得到的产物为二氧化碳、一氧化碳和水蒸气,将产生的气体按顺序通过装有无水氯化钙和氢氧化钠的硬质玻璃管,氢氧化钠管的质量增加了4.4g,则甲烷在标准状况下的体积是多少,无水氯化钙的质量增加了 ( )
| A. | 0.56L 1.8g | B. | 1.12L 3.6g | C. | 2.24L 1.8g | D. | 2.24L 3.6g |
1.我国提取中草药有效成分的常用溶剂有:水;或亲水性溶剂(如乙醇,与水互溶);或亲脂性溶剂(如乙醚,与水不互溶).诺贝尔奖获得者屠呦呦及其团队在提取青蒿素治疗疟疾过程中,记录如下:青蒿素的水煎剂无效;乙醇提取物的效用为30%~40%;乙醚提取物的效用为95%.下列推测不合理的是( )
| A. | 青蒿素在水中的溶解度很小 | B. | 青蒿素含有亲脂的官能团 | ||
| C. | 在低温下提取青蒿素,效果会更好 | D. | 乙二醇提取青蒿素的能力强于乙醚 |
2.化学与生产、生活密切相关.下列说法中正确的是( )
| A. | 油脂、糖类、蛋白质中产生能量最高的营养物质是蛋白质 | |
| B. | “从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| C. | 纯碱可用于制造玻璃,也可用于除去物品表面油污 | |
| D. | 废旧电池必须回收,主要目的是回收其中的金属 |