题目内容
5.如表是周期表的一部分,请回答有关问题.| ⅠA | ⅡA | ⅢA | Ⅳ | ⅤA | ⅥA | ⅦA | 0 | |
| 二周期 | ① | ② | | |||||
| 三周期 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
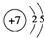 ,④的元素名称镁,②与⑦形成的化合物属于共价(填“离子”“共价”)化合物.
,④的元素名称镁,②与⑦形成的化合物属于共价(填“离子”“共价”)化合物.(2)原子半径③>④,金属性③>④,(填“>”或“<”)
(3)②和⑦形成的化合物中,能使品红溶液腿色的是SO2(填化学式),它对环境的主要危害是形成酸雨,⑦、⑧元素形成的氢化物热稳定性较强的是HCl(填化学式).
(4)写出③与水反应的化学方程式2Na+2H2O═H2↑+2NaOH.
分析 由元素在周期表中位置,可知①为N、②为O、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为S、⑧为Cl.
(1)①为N,原子核外有7个电子,有2个电子层,各层电子数为2、5;②与⑦形成的化合物为二氧化硫、三氧化硫;
(2)同周期自左而右原子半径减小、金属性减弱;
(3)②和⑦形成的化合物中,能使品红溶液腿色的是二氧化硫,它对环境的主要危害是形成酸雨;非金属性越强,对应氢化物越稳定;
(4)钠与水反应生成氢氧化钠与氢气.
解答 解:由元素在周期表中位置,可知①为N、②为O、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为S、⑧为Cl.
(1)①为N,原子核外有7个电子,有2个电子层,各层电子数为2、5,原子结构示意图为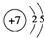 ,④的元素名称为镁,②与⑦形成的化合物为二氧化硫、三氧化硫,均属于共价化合物,
,④的元素名称为镁,②与⑦形成的化合物为二氧化硫、三氧化硫,均属于共价化合物,
故答案为: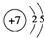 ;镁;共价;
;镁;共价;
(2)同周期自左而右原子半径减小、金属性减弱,故原子半径Na>Mg,金属性Na>Mg,
故答案为:>;>;
(3)②和⑦形成的化合物中,能使品红溶液腿色的是SO2,它对环境的主要危害是形成酸雨;非金属性Cl>S,非金属性越强,对应氢化物越稳定,故氢化物稳定性HCl>H2S,
故答案为:SO2;形成酸雨;HCl;
(4)钠与水反应生成氢氧化钠与氢气,反应方程式为:2Na+2H2O═H2↑+2NaOH,
故答案为:2Na+2H2O═H2↑+2NaOH.
点评 本题考查元素周期表与元素周期律,比较基础,注意对元素周期律的理解掌握.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
14.下列化合物中不能使酸性高锰酸钾溶液褪色的是( )
| A. | 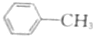 | B. | CH2═CHCH2OH | C. | 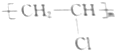 |
15.常温下,下列各组离子,在指定环境中一定能大量共存的是( )
| A. | pH<7的溶液中:Al3+、K+、SO32-、Cl- | |
| B. | 加入铝粉能放出氢气的溶液中:CO32-、AlO2-、I-、NO3- | |
| C. | 能使pH试纸变深蓝色的溶液中:S2-、SO32-、S2O32-、SO42- | |
| D. | 由水电离出的[OH-]=1×10-13mol/L的溶液中:Fe2+、NH4+、ClO-、Cl- |
13. 如表为元素周期表前四周期,其中的字母代表相应的元素.
如表为元素周期表前四周期,其中的字母代表相应的元素.
(1)元素h的二价阳离子的外围电子排布式为3d6.
(2)元素c、d、e、f的第一电离能(I1)由小到大的顺序为Al<Mg<O<N.(用相应元素的元素符号表示)
(3)表中所列的元素之间可以形成多种无机化合物和有机化合物,其中1mol苯甲醛分子(如图1)中含有σ键的数目为14NA此有机物中C原子的杂化类型为sp2.
(4)元素d与e形成的化合物常用于制作耐火材料.
(5)表中有关元素形成的一种离子和单质d3互为等电子体,则该离子的化学式为NO2-.
(6)已知j的晶胞结构如图2所示,又知j的密度为9.00g/cm3,则晶胞边长为$\root{3}{\frac{4×64}{9{N}_{A}}}$cm;jkd4常作电镀液,其中kd42-的空间构型是正四面体.k原子的杂化轨道类型是sp3.
 如表为元素周期表前四周期,其中的字母代表相应的元素.
如表为元素周期表前四周期,其中的字母代表相应的元素.| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | g | k | ||||||||||||||
| h | I | j |
(2)元素c、d、e、f的第一电离能(I1)由小到大的顺序为Al<Mg<O<N.(用相应元素的元素符号表示)
(3)表中所列的元素之间可以形成多种无机化合物和有机化合物,其中1mol苯甲醛分子(如图1)中含有σ键的数目为14NA此有机物中C原子的杂化类型为sp2.
(4)元素d与e形成的化合物常用于制作耐火材料.
(5)表中有关元素形成的一种离子和单质d3互为等电子体,则该离子的化学式为NO2-.
(6)已知j的晶胞结构如图2所示,又知j的密度为9.00g/cm3,则晶胞边长为$\root{3}{\frac{4×64}{9{N}_{A}}}$cm;jkd4常作电镀液,其中kd42-的空间构型是正四面体.k原子的杂化轨道类型是sp3.
20.4.6g纯净金属钠在干燥空气中被氧化后,得到7.0g固体,由此可判断其氧化产物是( )
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O2和Na2O | D. | 无法确定 |
10.某学生用碱式滴定管量取0.1mol•L-1的NaOH溶液,开始时仰视液面读数为1.0mL,取出部分溶液后,俯视液面,读数为11.00mL,该同学在操作中实际取出的液体体积为( )
| A. | 大于10.00mL | B. | 小于10.00Ml | C. | 等于10.00mL | D. | 不能确定 |
17.下列叙述不正确的是( )
| A. | 在镀件上电镀铜时,可用金属铜作阳极 | |
| B. | 镀层破损后,白铁(镀锌)比马口铁(镀锡)更易被腐蚀 | |
| C. | 工业上电解饱和食盐水制烧碱,用阳离子交换膜阻止OH-移向阳极 | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,完全相同的反应是负极反应 |
14.下列图中所示的实验操作评价合理的是( )
| A. | 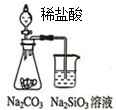 如图可能证明非金属性强弱:Cl>C>Si | |
| B. | 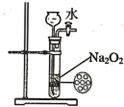 如图装置可用来制备少量氧气,并且控制反应的发生与停止 | |
| C. | 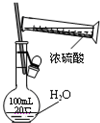 图中配制一定物质的量浓度的硫酸溶液不能直接在容量瓶中进行 | |
| D. | 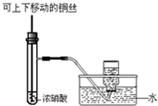 如图为制备并收集少量NO2气体 |
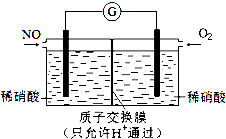 NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.
NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.