题目内容
13.硫酸在工业上有很多用途,但直接用浓硫酸具有危险性,所以经常需要将浓硫酸进行稀释后使用.现在实验室里有一瓶体积为500毫升,溶质质量分数为98%,密度为1.84克/毫升的浓硫酸.求:(1)该瓶浓硫酸中溶质的质量为多少克;
(2)取该硫酸100克稀释长9.8%的稀硫酸,需水多少毫升.
分析 (1)根据密度公式变形可求得溶液质量,再乘以溶质的质量分数即为该瓶浓硫酸中溶质的质量;
(2)利用98%的浓硫酸配制9.8%的稀硫酸,根据稀释前后溶液中硫酸的质量不变,可求得所加水的质量,然后可知水的体积.
解答 解:(1)由ρ=$\frac{m}{V}$可得,浓硫酸溶液质量m1=ρV=1.84g/cm3×500cm3=920g;
溶质的质量m=98%×920g=901.6g;
(2)设要加水的质量为m2,根据溶液稀释前后,溶质的质量不变,
100g×98%=9.8%(100g+m2)
解得m2=900g.
由ρ=$\frac{m}{V}$可得,所加水的体积V2=$\frac{{m}_{2}}{{ρ}_{水}}$=$\frac{900g}{1g/c{m}^{3}}$=900cm3=900ml.
答:(1)该瓶浓硫酸中溶质的质量为901.6g;
(2)取该硫酸100克稀释长9.8%的稀硫酸,需水900毫升.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、稀释前后溶质的质量不变,是正确解答本题的关键.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
1.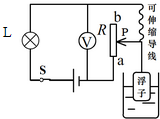 如图所示为某科技创新小组设计的水位计工作原理图,容器中的绝缘浮子随水位的升降带动滑动变阻器R的滑片P升降,并通过电压表V显示的数据来反应水位的升降情况.L是一个指示灯,电路各部分接触良好.当容器中的水位最低时,滑片P位于变阻器R的a端,则( )
如图所示为某科技创新小组设计的水位计工作原理图,容器中的绝缘浮子随水位的升降带动滑动变阻器R的滑片P升降,并通过电压表V显示的数据来反应水位的升降情况.L是一个指示灯,电路各部分接触良好.当容器中的水位最低时,滑片P位于变阻器R的a端,则( )
 如图所示为某科技创新小组设计的水位计工作原理图,容器中的绝缘浮子随水位的升降带动滑动变阻器R的滑片P升降,并通过电压表V显示的数据来反应水位的升降情况.L是一个指示灯,电路各部分接触良好.当容器中的水位最低时,滑片P位于变阻器R的a端,则( )
如图所示为某科技创新小组设计的水位计工作原理图,容器中的绝缘浮子随水位的升降带动滑动变阻器R的滑片P升降,并通过电压表V显示的数据来反应水位的升降情况.L是一个指示灯,电路各部分接触良好.当容器中的水位最低时,滑片P位于变阻器R的a端,则( )| A. | 当水位不变时,电压表V示数不变,指示灯L不亮 | |
| B. | 当水位上升时,电压表V示数变小,指示灯L变亮 | |
| C. | 当水位上升时,电压表V示数变大,指示灯L变暗 | |
| D. | 当水位下降时,电压表V示数变大,指示灯L变亮 |
18.小明要做“伏安法测电阻”的实验.
(1)请在方框内画出测量电路图

(2)将记录表格中的项目填写完整
(3)实验中电压表出现故障,小明有设计了如图所示电路(R0为已知电阻的定值电阻).且设计了如下实验步骤,请帮他把缺少的步骤补全,并写出Rx的表达式.实验步骤:
A、按照设计的电路图连接电路
B、断开S2,闭合S1记录电流表示数为I;
C、断开S1、闭合S2记录电流表示数为I2(或S1和S2都闭合记录电流表示数为I2)表达式:RX=$\frac{{I}_{1}}{{I}_{2}}$R0(或$\frac{{I}_{1}}{{I}_{2}-{I}_{1}}$R0)(用已知和测量的物理量的符号表示)
(1)请在方框内画出测量电路图

(2)将记录表格中的项目填写完整
| 实验次数 | 电流I/A | 电压U/V | 电阻R/Ω | |
A、按照设计的电路图连接电路
B、断开S2,闭合S1记录电流表示数为I;
C、断开S1、闭合S2记录电流表示数为I2(或S1和S2都闭合记录电流表示数为I2)表达式:RX=$\frac{{I}_{1}}{{I}_{2}}$R0(或$\frac{{I}_{1}}{{I}_{2}-{I}_{1}}$R0)(用已知和测量的物理量的符号表示)
2.中午站在阳光下的人发现影子在自己身体的右侧,那么他面对的方向是( )
| A. | 东方 | B. | 南方 | C. | 西方 | D. | 北方 |
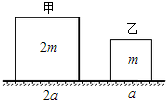 如图所示,置于水平地面上的实心均匀正方体甲、乙质量分别为2m和m,边长分别为2a和a.它们对地面的压强之比为1:2,实心均匀正方体丙、丁的密度和边长分别如表所示,若在丙或丁中选择一个叠放在甲或乙上方中央,使上方物体对下方物体的压强p与下方物体对地面的压强增加量△p的比值最大,应将丁叠放在甲上方中央.
如图所示,置于水平地面上的实心均匀正方体甲、乙质量分别为2m和m,边长分别为2a和a.它们对地面的压强之比为1:2,实心均匀正方体丙、丁的密度和边长分别如表所示,若在丙或丁中选择一个叠放在甲或乙上方中央,使上方物体对下方物体的压强p与下方物体对地面的压强增加量△p的比值最大,应将丁叠放在甲上方中央.