题目内容
甲、乙丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸反应,所得数据如下:
|
| 甲 | 乙 | 丙 |
| 取用金属混合物的质量(g) | 10 | 10 | 20 |
| 取用稀硫酸的质量(g) | 100 | 120 | 100 |
| 反应后过滤得到干燥固体的质量(g) | 2 | 2 | 12 |
计算:(1)金属混合物中铁的质量分数;
(2)甲制得硫酸亚铁的质量;
(3)该稀硫酸中溶质的质量分数。
解:甲与乙比较,乙的硫酸取量多,但金属剩余质量相等,说明剩余2g金属只有铜。甲与两比较,丙的金属取量多,但增多的金属质量没有任何减少,说明100g稀硫酸已经完全反应。由此可以确定,甲取的金属中铁与稀硫酸恰好反应安全。
(1)铁的质量:100g-2g=8g
金属混合物中铁的质量分数:
![]() ×100%=80%……………………………………………………1分
×100%=80%……………………………………………………1分
(2)设100g稀硫酸中溶质质量为x,反应生成的硫酸亚铁质量为y
Fe+H2SO4![]() FeSO4+H2↑
FeSO4+H2↑
56 98 152
8g x y
![]() =
=![]() x=14g
x=14g
![]() =
=![]() y=21.7g
y=21.7g
(3)稀硫酸中溶质的质量分数:
![]() ×100%=14%……………………………………………………1分
×100%=14%……………………………………………………1分

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
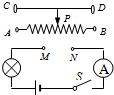 (2008?黄浦区一模)某实验小组甲、乙、丙三位同学,用相同的实验器材做电学实验.他们都按图所示的电路图连接电路,线头M、N可以分别与变阻器的接线柱A、B、C、D中的任意两个相接,实验中,由于甲、乙丙三位同学连接变阻器接线柱的方法不同,甲同学不论怎样移动变阻器滑片P,灯泡亮度不变,且较暗;
(2008?黄浦区一模)某实验小组甲、乙、丙三位同学,用相同的实验器材做电学实验.他们都按图所示的电路图连接电路,线头M、N可以分别与变阻器的接线柱A、B、C、D中的任意两个相接,实验中,由于甲、乙丙三位同学连接变阻器接线柱的方法不同,甲同学不论怎样移动变阻器滑片P,灯泡亮度不变,且较暗;