下列方程中是关于x的一元二次方程的是( ▲ )
A.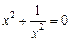 | B.ax2+bx+c=0 | C.(x-1)(x-2)=1 | D.3x2-2xy-5y2=0 |
如果△ABC中,sin A=cos B=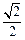 ,则下列最确切的结论是( ▲ )
,则下列最确切的结论是( ▲ )
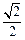 ,则下列最确切的结论是( ▲ )
,则下列最确切的结论是( ▲ )| A.△ABC是直角三角形 | B.△ABC是等腰三角形 |
| C.△ABC是等腰直角三角形 | D.△ABC是锐角三角形 |
下列玻璃仪器洗涤方法正确的是 ( )


| A.做银镜反应后的试管用氨水洗涤 | B.做碘升华实验后的烧杯用酒精洗涤 |
| C.盛装苯酚后的试管用盐酸洗涤 | D.用KClO3和MnO2制取O2后的试管用水洗涤 |
有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在30 mL处,把管中的溶液全部放出,承接在量筒中溶液的体积是
| A.等于30mL | B.等于20mL | C.大于20mL | D.大于30mL |
(12分)某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度(酸度单位:g/100ml),现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定。下表是4种常见指示剂的变色范围:
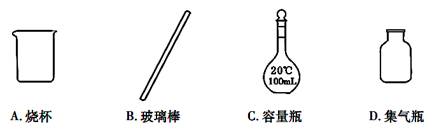
(1)该实验应选用 作指示剂,向锥形瓶中移取一定体积的白醋所用的仪器是 。
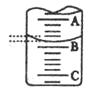
(2)下图表示50ml滴定管中液面的位置,若A与C刻度间相差1ml,A处的刻度为25,滴定管中液面读数为 ml。此时滴定管中液体的体积 。
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为Vml,NaOH标准液浓度为C mol/L,三次实验结果记录如下:
从上表可以看出,第一次实验中记录消耗NaOH溶液体积明显多于后两次,其原因可能
是
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
E.滴定NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中总酸度的表达式(可以不必化简):
(酸度:每100ml溶液中含有溶质酸的质量,单位:g/100ml)
| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(PH) | 5.0-8.0 | 3.1-4.4 | 4.4-6.2 | 8.2-10.0 |
(2)下图表示50ml滴定管中液面的位置,若A与C刻度间相差1ml,A处的刻度为25,滴定管中液面读数为 ml。此时滴定管中液体的体积 。

(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为Vml,NaOH标准液浓度为C mol/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/ml | 26.02 | 25.32 | 25.28 |
是
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
E.滴定NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中总酸度的表达式(可以不必化简):
(酸度:每100ml溶液中含有溶质酸的质量,单位:g/100ml)
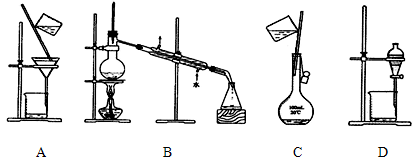
以下实验操作正确的是( )
| A.用量筒量取5.0mL浓硫酸并直接在量筒中稀释 |
| B.称量NaOH固体时,将药品直接放在托盘上 |
| C.给烧瓶里的液体加热时,垫上石棉网 |
| D.用嘴吹灭燃着的酒精灯火焰 |
下列实验不能达到目的的是( )
0 112000 112008 112014 112018 112024 112026 112030 112036 112038 112044 112050 112054 112056 112060 112066 112068 112074 112078 112080 112084 112086 112090 112092 112094 112095 112096 112098 112099 112100 112102 112104 112108 112110 112114 112116 112120 112126 112128 112134 112138 112140 112144 112150 112156 112158 112164 112168 112170 112176 112180 112186 112194 366461
| A.往酸性KMnO4溶液中通入乙烯验证乙烯的还原性 |
| B.用二氧化锰和浓盐酸反应制取氯气 |
| C.加热氯化铵与氢氧化钙固体混合物制取氨气 |
| D.用植物油萃取溴水中的溴 |