根据溶液的组成填写下表(①~④填物质的化学式)
| 溶液 | 稀盐酸 | 医用酒精 |
| 溶质 | ①________ | ③________ |
| 溶剂 | ②________ | ④________ |
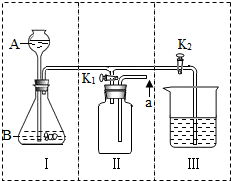 如图是某小组设计的可用于制备并验证CO2性质的装置.
如图是某小组设计的可用于制备并验证CO2性质的装置.
①写出仪器A和B的名称:A________;B________;
②写出实验室制取CO2的化学反应方程式________;
③小组同学对装置进行气密性检查完好后,打开K1、关闭K2时,开始制备CO2.装置Ⅰ中的现象________;装置Ⅰ和Ⅱ组合使用能否控制Ⅰ中反应的进行,请写出理由________;
④实验中,同学们将________的木条放在a处,木条熄灭.关闭K1,瓶内CO2按如图操作实际不能集满,请从上图装置分析原因________.为能集满CO2,你的改进方法是________;
⑤利用Ⅰ、Ⅲ装置组合,当打开K2、关闭K1时,可验证CO2的有关性质.请完成下列表格
| 装置中物质 | 实验现象 | 实验结论 |
| (11) | (12) | 与水反应 |
| (13) | 变浑浊 | (14) |
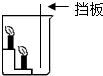 (替换装置,从烧杯挡板右侧通入CO2 (替换装置,从烧杯挡板右侧通入CO2 | (15) | (16) |
铜是一种常用的金属,纯净的铜颜色为紫红色,它能够和硝酸银溶液发生化学反应,生成硝酸铜和银单质.某同学设计下表所示实验,探究金属铜对过氧化氢溶液分解速率的影响.
| 操作 | 装置 | 现象 |
| 1、取一小块铜丝网,卷成筒形,固定在铜丝上. |  | |
| 2、分别向①和②中注入15mL、30%的H2O,并放入盛有热水的③中. | 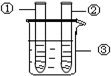 | 约1min后可观察到①和②中都有少量气泡产生 |
| 3、把铜丝插入①中. | 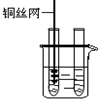 | ①中有大量气泡产生,约5min后不再有气泡产生;此时②中仍然有少量气泡产生 |
(2)根据上述实验,可以得出的结论是______;
(3)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是______.
A.称量实验前铜丝网的质量 B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰 D.将实验后的铜丝网插入AgNO3溶液中.
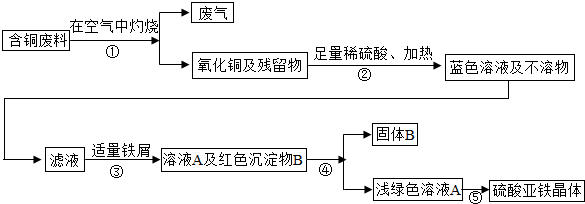
 2CuSO4+2H2O),该方案明显优于原方案,你认为优点是______.现有160kg含铜80%的废料,完全与硫酸、氧气发生反应,最多生成CuSO4______kg.
2CuSO4+2H2O),该方案明显优于原方案,你认为优点是______.现有160kg含铜80%的废料,完全与硫酸、氧气发生反应,最多生成CuSO4______kg.