下表是氯化钾和硝酸钾在不同温度时的溶解度
|
温度/℃ |
O |
20 |
40 |
60 |
80 |
|
|
溶解度/g |
KCl |
27.6 |
34.O |
40.0 |
45.5 |
51.1 |
|
KN03 |
13.3 |
31.6 |
63.9 |
1lO |
169 |
(1)从表中数据可以看出影响物质溶解度的因素之一是 ;
(2)根据数据表,在答题卷的图中绘制硝酸钾的溶解度曲线;
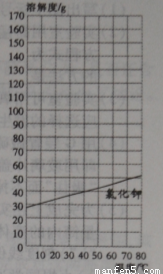
(3)从溶解度曲线上查出:45℃时,氯化钾的溶解度为 g;
(4)据图分析,要除去硝酸钾中混有的少量氯化钾,可采用的结晶方法是 。
小煜同学通过学习知道,乙醇汽油是一种新型车用燃料,于是他对汽油中添加乙醇的目的进行了如下探究。
【猜想】 猜想l:可以减少汽车尾气的污染;
猜想2:可以产生更多的热量,增强汽车的动力。
【诒计与实验】
|
序号 |
实验步骤 |
实验现象 |
结论 |
|
I
|
在两个蒸发皿中各加入lOmL 冷水,控制相同燃烧条件,分别用 乙醇和汽油作为燃料进行加热,记 录从开始加热到水沸腾的时间。 |
用乙醇加热耗时118s;
用汽油加热耗时56s。
|
猜想2 (填“成立"或 “不成立"); |
|
Ⅱ
|
实验l停止加热后,取下蒸发 皿,观察蒸发皿的底部。
|
用乙醇加热的蒸发皿底部 只有极少量炭黑,而用汽油加热 的蒸发皿底部有大量炭黑。 |
(可仿照上格填写)
|
【分析与讨论】
(1)实验I是一个对比实验,实验过程中不一定要控制的条件是 (填序号);
A.水的初始温度必须相同 B.加热开始计时点必须相同
C.燃具产生火焰的大小必须相同 D.蒸发皿的大小必须相同
(2)汽车的发动机、排气管等部件易出现积炭,使用乙醇汽油后,这些部件产生的积炭量将 ;
(3)目前乙醇汽油中乙醇的添加量约为10%.可一定程度节省石油资源。结合实验I的结论分析,如果乙醇的添加量过大,会使汽车动力 (填“增强"、“减弱"或“不变")。
某实验小组开展了如下有关碱的化学性质探究活动:
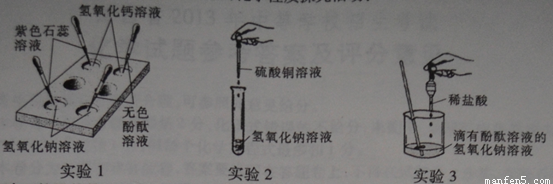
(1)买验l的目的是 ;
(2)实验2中发生反应的化学方程式是 ;
(3)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含
有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。
小萍加入的试剂可能是 ;
(4)通过上述实验探究活动,可以总结出碱的化学性质是:
①碱能与酸发生中和反应(精校);
② ;
…………
(5)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,该两瓶溶液的溶质质量分数分别为5%和l0%。请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)。
|
实验步骤 |
预计现象及相应结论 |
|
|
为5%的氢氧化钠溶液,另一种为l0%的氢氧化钠溶液。 |

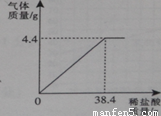
 2Fe+3C02,该反应中体现了C0具有 性;
2Fe+3C02,该反应中体现了C0具有 性;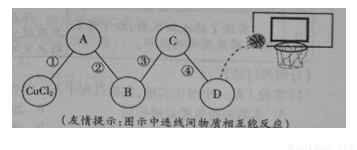
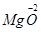 D.H2O2
D.H2O2 CuO
CuO 2AlO
2AlO