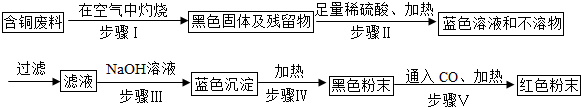
为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了如下甲、乙两个实验方案.
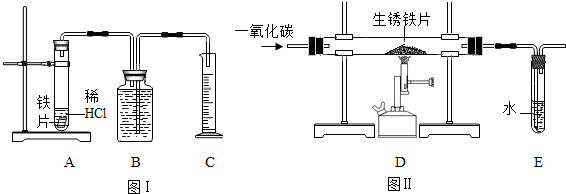
方案甲:称得生锈铁片的质量为m1g,按图Ⅰ所示装置进行实验.完全反应后,测得室温下产生氢气的体积为V1L,查得其密度为ρg/L.
方案乙:称得生锈铁片的质量为m2g,先按图Ⅱ所示装置进行实验.当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温.取出铁片,按图Ⅰ所示装置继续进行实验.完全反应后,测得室温下产生氢气的体积为V2L,查得其密度为ρg/L.
(1)【评价交流】有同学分析甲方案即使读数准确也不可行,你认为其缺陷是:______.
(2)【设计实验】方案乙中,同学们设计了如下实验报告,请帮助完成.
| 实验编号 | 实验步骤 | 实验现象 | 解释或化学方程式 |
①装置Ⅱ | 通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 | 反应结束后,还要继续通CO至室温的目的是______. |
| ②装置Ⅰ | 将光亮铁片放入稀盐酸中,完全反应 | 溶液颜色由无色变成浅绿色,有气泡放出 | 化学方程式:______ |
(4)【结论】生锈铁片中铁元素的质量分数是______(用字母表示)
食盐和纯碱(Na2CO3?10H2O)的溶解度如表:
| 0℃ | 10℃ | 20℃ | 30℃ | |
| NaCl/g | 35.7 | 35.8 | 36.0 | 36.3 |
| Na2CO3?10H2O/g | 7 | 12.5 | 21.6 | 38.8 |
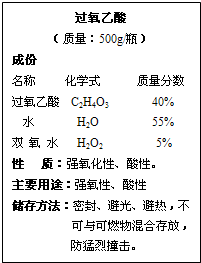 某市售过氧乙酸(化学式为:C2H4O3),其标签上的部分文字说明如图.请回答:
某市售过氧乙酸(化学式为:C2H4O3),其标签上的部分文字说明如图.请回答:
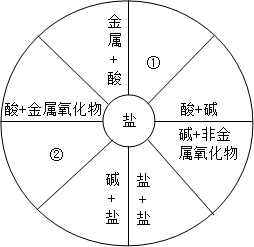 小梅同学学习了单质、氧化物、酸、碱、盐性质后,发现许多不同类别的物质反应时能生产盐,于是她构建了如图所示的知识网络图.
小梅同学学习了单质、氧化物、酸、碱、盐性质后,发现许多不同类别的物质反应时能生产盐,于是她构建了如图所示的知识网络图.