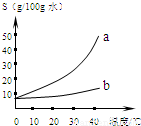
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
(1)Na2CO3溶解度曲线为 (填“a”或“b”).
(2)要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法是 (填写编号).
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是 .
(4)40℃时的100g Na2CO3的饱和溶液中含有 g溶质,该溶液的溶质质量分数为 %.(计算结果精确到0.1)
(5)若将30%的碳酸钠溶液100g,稀释到10%,需要加水 mL.
0 87366 87374 87380 87384 87390 87392 87396 87402 87404 87410 87416 87420 87422 87426 87432 87434 87440 87444 87446 87450 87452 87456 87458 87460 87461 87462 87464 87465 87466 87468 87470 87474 87476 87480 87482 87486 87492 87494 87500 87504 87506 87510 87516 87522 87524 87530 87534 87536 87542 87546 87552 87560 211419
(1)Na2CO3溶解度曲线为 (填“a”或“b”).
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(3)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是 .
(4)40℃时的100g Na2CO3的饱和溶液中含有 g溶质,该溶液的溶质质量分数为 %.(计算结果精确到0.1)
(5)若将30%的碳酸钠溶液100g,稀释到10%,需要加水 mL.