如图是某学生绘制的元素周期表的一部分:
请根据相关信息与知识回答:
(1)该表中元素化学性质不活泼的有 ;(只写一种)
(2)请写出原子序数分别为8、13两种元素组成的化合物的化学式 ;
(3)仔细阅读和观察上表,其中有一种常见元素的元素名称书写有误,请写出其正确的元素名称 ,过量排放该元素的一种氧化物到大气中,会引起 效应,使全球变暖,请列举至少一条防止该效应进一步增强的措施 .

| 1H 氢 | 2He 氦 | ||||||
| 3Li 锂 | 4Be 铍 | 5B 硼 | 6C 炭 | 7N 氮 | 8O 氧 | 9F 氟 | 10Ne 氖 |
| 11Na 钠 | 12Mg 镁 | 13Al 铝 | 14Si 硅 | 15P 磷 | 16S 硫 | 17Cl 氯 | 18Ar 氩 |
(1)该表中元素化学性质不活泼的有 ;(只写一种)
(2)请写出原子序数分别为8、13两种元素组成的化合物的化学式 ;
(3)仔细阅读和观察上表,其中有一种常见元素的元素名称书写有误,请写出其正确的元素名称 ,过量排放该元素的一种氧化物到大气中,会引起 效应,使全球变暖,请列举至少一条防止该效应进一步增强的措施 .

为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
(1)第2次测得剩余固体质量为74g,其成分为______.
A.铜 B.锌 C.铜和锌
(2)该黄铜样品中铜和锌的质量比m铜:m锌:______.
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图.______.
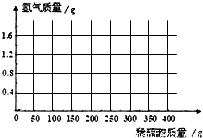
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
A.铜 B.锌 C.铜和锌
(2)该黄铜样品中铜和锌的质量比m铜:m锌:______.
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图.______.

2010年5月12日,在苍茫海水中沉没了800多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑.已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3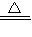 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.
实验用到的主要装置为:

(1)装置连接顺序为:______.(填写编号)
(2)操作步骤及数据处理:
第一步 检查气密性;
第二步 装入药品,称取装置①和③的质量;
第三步 试验后再次称取装置①和③的质量,记录数据如表;
根据以上数据可得产生的水和二氧化碳的质量之比为______.(要求写出最简整数比)
(3)结果分析;从下列选项中选出产生该实验结果可能的原因有哪些?______.
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解.
0 85270 85278 85284 85288 85294 85296 85300 85306 85308 85314 85320 85324 85326 85330 85336 85338 85344 85348 85350 85354 85356 85360 85362 85364 85365 85366 85368 85369 85370 85372 85374 85378 85380 85384 85386 85390 85396 85398 85404 85408 85410 85414 85420 85426 85428 85434 85438 85440 85446 85450 85456 85464 211419
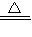 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.
实验用到的主要装置为:

(1)装置连接顺序为:______.(填写编号)
(2)操作步骤及数据处理:
第一步 检查气密性;
第二步 装入药品,称取装置①和③的质量;
第三步 试验后再次称取装置①和③的质量,记录数据如表;
质 装置 量 时间 | 装置① | 装置③ |
| 实验前 | 220.0克 | 195.0克 |
| 实验后 | 222.1克 | 199.4克 |
(3)结果分析;从下列选项中选出产生该实验结果可能的原因有哪些?______.
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解.
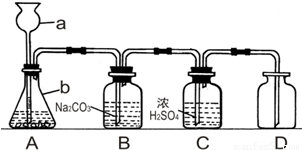 实验室常用石灰石和稀盐酸制取二氧化碳气体,在收集到的气体里含有少量的氯化氢气体和水蒸气,要得到干燥纯净的二氧化碳气体,可用下列装置来制取二氧化碳,请回答下列问题:
实验室常用石灰石和稀盐酸制取二氧化碳气体,在收集到的气体里含有少量的氯化氢气体和水蒸气,要得到干燥纯净的二氧化碳气体,可用下列装置来制取二氧化碳,请回答下列问题: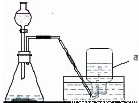 如图是实验室制取气体的常用装置.
如图是实验室制取气体的常用装置.

