气体的实验室制法是一种重要的实验基本技能,请回顾二氧化碳的实验室制法,回答下列问题:
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2 CO2
CO2
②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4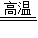 CaO+CO↑+CO2↑
CaO+CO↑+CO2↑
⑤CO+Fe2O3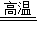 2Fe+3CO2
2Fe+3CO2
…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:______.现提供有①纯净的CaCO3白色粉末,②大理石,③稀盐酸,③浓盐酸,④稀硫酸,⑤浓硫酸.其中最适合用于实验室制取二氧化碳的药品是______(填代号)
(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
①分析上述数据可得到一个结论:______;盐酸是氯化氢气体溶于水得到的溶液,升高盐酸溶液的温度,其密度将变______.
②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸______ml.配制过程中要用到量筒、______、烧杯、玻璃棒等仪器.
(3)下面是二氧化碳的制取、净化、收集和量气的相关实验
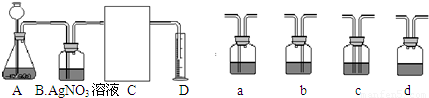
(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是______
②实验过程B装置产生的主要实验现象是:______;
涉及化学反应是______.
③方线框中的C装置应该选择上面提供的a、b、c、d的______.
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2
 CO2
CO2②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4
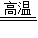 CaO+CO↑+CO2↑
CaO+CO↑+CO2↑⑤CO+Fe2O3
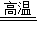 2Fe+3CO2
2Fe+3CO2…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:______.现提供有①纯净的CaCO3白色粉末,②大理石,③稀盐酸,③浓盐酸,④稀硫酸,⑤浓硫酸.其中最适合用于实验室制取二氧化碳的药品是______(填代号)
(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸______ml.配制过程中要用到量筒、______、烧杯、玻璃棒等仪器.
(3)下面是二氧化碳的制取、净化、收集和量气的相关实验

(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是______
②实验过程B装置产生的主要实验现象是:______;
涉及化学反应是______.
③方线框中的C装置应该选择上面提供的a、b、c、d的______.
小军家的下水管道堵了.爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了.小军对此很好奇,于是想探究“管道通”中的物质成分.
【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下.
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道.
(3)铝粉为银灰色固体.铝与酸、碱溶液都能反应放出氢气,反应时放出大量热.
①铝与盐酸反应的化学方程式是______.
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+______═2NaAlO2+3H2↑
【猜想与验证】小军打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
(1)猜想:白色固体颗粒为氢氧化钠.
结论:白色固体颗粒为氢氧化钠.
(2)猜想:银灰色粉末为铝粉.
结论:银灰色粉末为铝粉.
【应用】
使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口.一会儿,管道内发生化学反应.根据题目信息,推测管道内的反应现象是______.
【反思】
①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似.要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在.
②根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)______.

【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下.
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道.
(3)铝粉为银灰色固体.铝与酸、碱溶液都能反应放出氢气,反应时放出大量热.
①铝与盐酸反应的化学方程式是______.
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+______═2NaAlO2+3H2↑
【猜想与验证】小军打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
| 实验操作 | 实验现象 |
| 1照下图安装两套仪器. 2 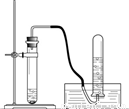 | |
| ②两套仪器中分别依次加入银灰色粉末和稀盐酸;银灰色粉末和______. | 都产生大量无色气体,试管外壁温度明显升高. |
| ③待导管口有气泡均匀持续冒出时,收集1试管气体,验纯.(两套仪器操作相同) | 验纯时的操作和现象:(两套仪器相同) 用拇指堵住集满氢气的试管口,靠近火焰,移开拇指点火,声音很小(或有噗的一声). |
| ④在导管口点燃气体.(两套仪器操作相同) | 都产生淡蓝色火焰. |
结论:白色固体颗粒为氢氧化钠.
(2)猜想:银灰色粉末为铝粉.
实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿. | 白色固体颗粒表面潮湿并逐渐溶解. |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁. | ______. |
| ③向步骤②得到的溶液中放入一段羊毛线,加热一段时间. | 羊毛线逐渐消失. |
【应用】
使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口.一会儿,管道内发生化学反应.根据题目信息,推测管道内的反应现象是______.
【反思】
①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似.要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在.
②根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)______.

某校化学小组的同学想探究生铁中碳的含量,他们取组成完全相同的三份生铁(假设生铁中只含铁和碳),分别加入50g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后得到下表的实验数据:请计算:(计算结果精确到0.1%):
(1)该生铁中碳的质量分数为______.
(2)所用稀硫酸的溶质质量分数是多少?
| 实验次数 | 实验I | 实验Ⅱ | 实验Ⅲ |
| 生铁的质量 | 2.9g | 5.8g | 7.2g |
| 氢气的质量 | 0.1g | 0.2g | 0.2g |
(2)所用稀硫酸的溶质质量分数是多少?
实验测得某些食物的近似pH如下,下列说法正确的是( )
A.牛奶和玉米粥均属于碱性食物
B.胃酸过多的人应少食泡菜
C.番茄的酸性比苹果强
D.用湿润的pH试纸蘸取葡萄汁测其pH
0 85249 85257 85263 85267 85273 85275 85279 85285 85287 85293 85299 85303 85305 85309 85315 85317 85323 85327 85329 85333 85335 85339 85341 85343 85344 85345 85347 85348 85349 85351 85353 85357 85359 85363 85365 85369 85375 85377 85383 85387 85389 85393 85399 85405 85407 85413 85417 85419 85425 85429 85435 85443 211419
| 食物 | 泡菜 | 葡萄 | 番茄 | 苹果 | 牛奶 | 玉米粥 |
| pH | 3.4 | 4.2 | 4.4 | 3.1 | 6.5 | 7.8 |
A.牛奶和玉米粥均属于碱性食物
B.胃酸过多的人应少食泡菜
C.番茄的酸性比苹果强
D.用湿润的pH试纸蘸取葡萄汁测其pH
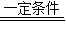 CH3OCH3+H2O,则X的化学式为( )
CH3OCH3+H2O,则X的化学式为( )