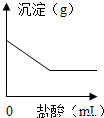
为探究“酸碱中和反应”,进行了如下研究.
【实验原理】将稀HCl滴入盛有NaOH溶液的烧杯中,反应的化学方程式为______;
【提出问题】实验中未观察到明显现象,同学们对该反应是否发生提出了疑问:反应后溶液中溶质是什么?
【假设猜想】溶液中的溶质有氯化钠,还可能有:
猜想1:HCl
猜想2:NaOH
猜想3:HCl和NaOH
你认为上述猜想不合理的是______.
【实验方案】(1)某同学用一支洁净试管取少量烧杯中的溶液,滴加FeCl3溶液,无明显现象,说明烧杯中溶液里一定不含______;
(2)为了验证其余猜想,各小组进行如下三个方案的探究.
【推论与分析】上述实验方案中有两处明显错误:
①实验操作中的错误是______;
②实验结论中也有一个是错误的,错误的原因是______;
通过对上述实验的正确操作,同学们得出了正确的结论.
你认为【假设猜想】中______是正确的.
(3)在20g10%的氢氧化钠溶液中加入25g稀盐酸恰好完全反应.
①计算氢氧化钠的物质的量为______;
②计算25g稀盐酸中溶质的质量分数______(计算结果精确到0.1%).(根据化学方程式列式计算)
0 81219 81227 81233 81237 81243 81245 81249 81255 81257 81263 81269 81273 81275 81279 81285 81287 81293 81297 81299 81303 81305 81309 81311 81313 81314 81315 81317 81318 81319 81321 81323 81327 81329 81333 81335 81339 81345 81347 81353 81357 81359 81363 81369 81375 81377 81383 81387 81389 81395 81399 81405 81413 211419
【实验原理】将稀HCl滴入盛有NaOH溶液的烧杯中,反应的化学方程式为______;
【提出问题】实验中未观察到明显现象,同学们对该反应是否发生提出了疑问:反应后溶液中溶质是什么?
【假设猜想】溶液中的溶质有氯化钠,还可能有:
猜想1:HCl
猜想2:NaOH
猜想3:HCl和NaOH
你认为上述猜想不合理的是______.
【实验方案】(1)某同学用一支洁净试管取少量烧杯中的溶液,滴加FeCl3溶液,无明显现象,说明烧杯中溶液里一定不含______;
(2)为了验证其余猜想,各小组进行如下三个方案的探究.
| 实验方案 | 甲 | 乙 | 丙 |
实验操作 | 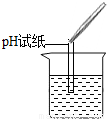 | 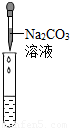 | 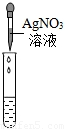 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | ______ | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
①实验操作中的错误是______;
②实验结论中也有一个是错误的,错误的原因是______;
通过对上述实验的正确操作,同学们得出了正确的结论.
你认为【假设猜想】中______是正确的.
(3)在20g10%的氢氧化钠溶液中加入25g稀盐酸恰好完全反应.
①计算氢氧化钠的物质的量为______;
②计算25g稀盐酸中溶质的质量分数______(计算结果精确到0.1%).(根据化学方程式列式计算)