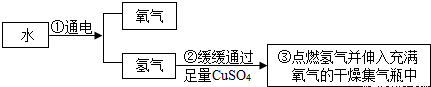
控制变量是种重要的实验方法.能达到实验目的方案是( )
A.A
B.B
C.C
D.D
| A、探究反应物接触面积对反应速率的影响 | B、比较20℃时硝酸钾和氯化钠的溶解性(两者均易溶于水) | C、探究反应物浓度对反应速率的影响 | D、探究燃烧的温度是否须达到着火点(白磷着火点:40℃) |
 |  |  |  |
A.A
B.B
C.C
D.D
KNO3和NaCl是日常生产生活中常见的两种盐.
①在农业生产中, 是种常见的复合肥.
②食盐是最常用的调味品.炒菜时不小心将食盐洒在火焰上,可观察到火焰呈 色.
③下表是KNO3和NaCl的溶解度.
I.0℃时,KNO3的溶解度是 g/100g水.
II.“海水晒盐”是获得食盐晶体(粗盐)的主要方法,选择这种结晶方法的依据是 .
Ⅲ.在不改变溶液浓度的条件下,将接近饱和的KNO3溶液变为饱和所采用的方法是 .
IV.当温度在 (填相邻温度范围)时,能够配制浓度相等的KNO3和NaCl的饱和溶液.
①在农业生产中, 是种常见的复合肥.
②食盐是最常用的调味品.炒菜时不小心将食盐洒在火焰上,可观察到火焰呈 色.
③下表是KNO3和NaCl的溶解度.
| ||||||||||||||||||||
II.“海水晒盐”是获得食盐晶体(粗盐)的主要方法,选择这种结晶方法的依据是 .
Ⅲ.在不改变溶液浓度的条件下,将接近饱和的KNO3溶液变为饱和所采用的方法是 .
IV.当温度在 (填相邻温度范围)时,能够配制浓度相等的KNO3和NaCl的饱和溶液.
课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数.
【化学方法】向一定量氯化钠溶液中加入足量硝酸银溶液,得到0.02mol氯化银固体,则该氯化钠溶液中氯化钠的质量为①______g(根据化学方程式列式计算).
经多次实验测定,该溶液的溶质质量分数为10%.
【物理方法】取一定量该溶液进行蒸发,测量实验数据如下:
若化学方法测定结果准确,则物理方法测定结果产生误差的原因是③______
A.蒸发时未用玻璃棒搅拌 B.所取氯化钠溶液质量偏大
C.蒸发时出现少量晶体时就停止加热 D.实验后未将玻璃棒上的白色固体移入蒸发皿.
【化学方法】向一定量氯化钠溶液中加入足量硝酸银溶液,得到0.02mol氯化银固体,则该氯化钠溶液中氯化钠的质量为①______g(根据化学方程式列式计算).
经多次实验测定,该溶液的溶质质量分数为10%.
【物理方法】取一定量该溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) | 25.0g |
| 蒸发皿+食盐溶液(g) | 45.0g |
| 蒸发皿+食盐晶体(g) | 27.4g |
| 数据处理 | 溶液的溶质质量分数为②______ |
A.蒸发时未用玻璃棒搅拌 B.所取氯化钠溶液质量偏大
C.蒸发时出现少量晶体时就停止加热 D.实验后未将玻璃棒上的白色固体移入蒸发皿.
对比学习有利于发现事物的共性与个性.为探究酸的性质,同学们进行了如下实验.
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀.请分析上述现象并回答:
Ⅰ.废液缸中产生气体的反应的化学方程式为______.
Ⅱ.废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有______(填化学式).
0 81173 81181 81187 81191 81197 81199 81203 81209 81211 81217 81223 81227 81229 81233 81239 81241 81247 81251 81253 81257 81259 81263 81265 81267 81268 81269 81271 81272 81273 81275 81277 81281 81283 81287 81289 81293 81299 81301 81307 81311 81313 81317 81323 81329 81331 81337 81341 81343 81349 81353 81359 81367 211419
| 实验内容 | 实验现象 | 分析与结论 |
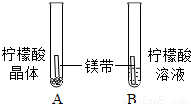 | A试管内______,B试管中镁带表面冒气泡. | 酸的很多反应通常在水溶液中才能完成. |
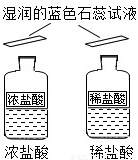 | ______(填“浓”或“稀”)盐酸瓶口的蓝色石蕊试纸很快变红. | 即使是同种酸,由于 ______不同,它们的性质不完全相同. |
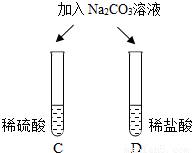 | 两试管中均产生______ | 不同的酸具有相似的性质,这是因为酸的组成中都含有______(填元素符号). |
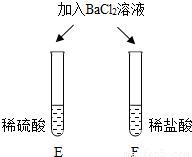 | E试管中产生______, F试管中无明显现象. | 不同的酸根会导致酸的“个性”差异.因此,可用氯化钡溶液鉴别盐酸和硫酸. |
Ⅰ.废液缸中产生气体的反应的化学方程式为______.
Ⅱ.废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有______(填化学式).