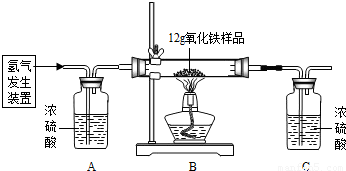
某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3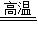 2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
得到如下数据:
(1)请计算样品中氧化铁的质量分数.(写出计算步骤,计算结果精确到0.l%)
(2)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为______(不用化简);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会______(选填“偏大”、“偏小”或“不变”).
0 79516 79524 79530 79534 79540 79542 79546 79552 79554 79560 79566 79570 79572 79576 79582 79584 79590 79594 79596 79600 79602 79606 79608 79610 79611 79612 79614 79615 79616 79618 79620 79624 79626 79630 79632 79636 79642 79644 79650 79654 79656 79660 79666 79672 79674 79680 79684 79686 79692 79696 79702 79710 211419
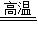 2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:得到如下数据:
| 装置 | B | C |
| 反应前质量 | 86.3g | 284.2g |
| 反应后质量 | 83.9g | 286.9g |
(2)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为______(不用化简);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会______(选填“偏大”、“偏小”或“不变”).





